Die Friedel-Crafts Alkylierung dient der Darstellung von Alkylaromaten mit Hilfe von Alkylhalogeniden. Für diese elektrophile Substitution ist ein Katalysator von Nöten der die Kohlenstoff-Halogenid-Bindung weiter polarisiert - dafür eignen sich katalytische Mengen von Lewissäuren. Weitere Alkylierungsmittel können Alkohole und Alkene sein. Die Reaktion ist reversibel.
Benannt nach: Charles Friedel und James Crafts (F & USA)
Entdeckung: 1877
Mechanismus:
Die Reaktion benötigt Lewissäuren, wie AlCl3 oder AlBr3 als Katalysator, diese schwächen die Bindungen zwischen dem Halogenid und dem Alkylrest und erhöhen die partiell positive Ladung auf letzterem. Der Grad der Polarisierung hängt vom Katalysator und dem Alkylrest ab; im Extremfall bildet sich ein Carbenium-Ion. Das elektrophile Agens ist normalerweise ein Komplex aus dem Halogenid und der Lewissäure:
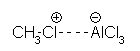
Zunächst reagiert der Aromat unter Addition des Elektrophils:
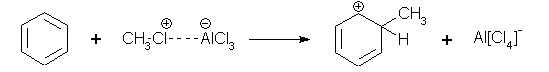
Anschließend wird das Proton abgespalten und der Aromat rearomatisiert (und wieder stabilisiert):
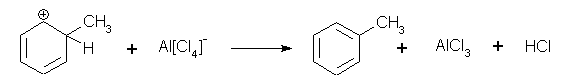
Die Friedel-Carfts Alkylierung funktioniert nicht am deaktiviertem Aromaten, desweiteren wird die Reaktion von einer Reihe von Problemen eingeschränkt: Es besteht die Möglichkeit einer Mehrfachalkylierung sowie einer Umlagerung in der Seitenkette. Diese oft unerwünschten Reaktionen senken den präparativen Nutzen.