Vanillin ist allseits bekannt und der weltweit am öftesten verwendete Aromastoff. Er findet sich natürlich in den Kapselfrüchten der Gewürzvanille (Vanilla planifolia), aber auch in anderen Vanillesorten wie der Tahiti-Vanille. Vanillin wird dort aus seiner olfaktorisch inaktiven Glykosid-Form freigesetzt und kann erst dann seine Wirkung entfalten. Die Nutzung natürlichen Vanillins ist sehr lang zurückverfolgbar, die Herstellung von künstlichem, synthetischem Vanillin ist aber eine Entwicklung der modernen Zeit. Vanillin, oder chemisch auch 4-Hydroxy-3-methoxybenzaldehyd, ist ein phenolischer Aldehyd mit charakteristischem Geruch. Es kann unter anderem aus Coniferin, Eugenol (welches wiederum in Nelken vorkommt), Guajacol oder aus Holz (Ligninsulfonate) hergestellt werden.
Obwohl Vanillin aufgrund der Massenproduktion sehr günstig ist, interessiert man sich in der Lebensmittelindustrie und der Parfümerie nicht nur für Vanillin selbst, sondern auch für seine Derivate. Tauscht man die 3-Methoxygruppe des Vanillins gegen eine 3-Ethoxygruppe aus, gelangt man zum künstlich hergestellten Ethylvanillin. Dieses hat einen ähnlichen, aber deutlich intensiveren und blumigeren Geruch als seine Stammverbindung. Da es olfaktorisch 3-4x potenter ist, wird es zum Aromatisieren von Schokolade und vielen anderen Lebensmitteln eingesetzt. In billigen Lebensmitteln ist meist entweder synthetisches Vanillin oder Ethylvanillin enthalten. Echte Vanille liegt preislich deutlich über der künstlichen Alternative und wird daher eher entweder nur in teureren oder speziell beworbenen Produkten verwendet.
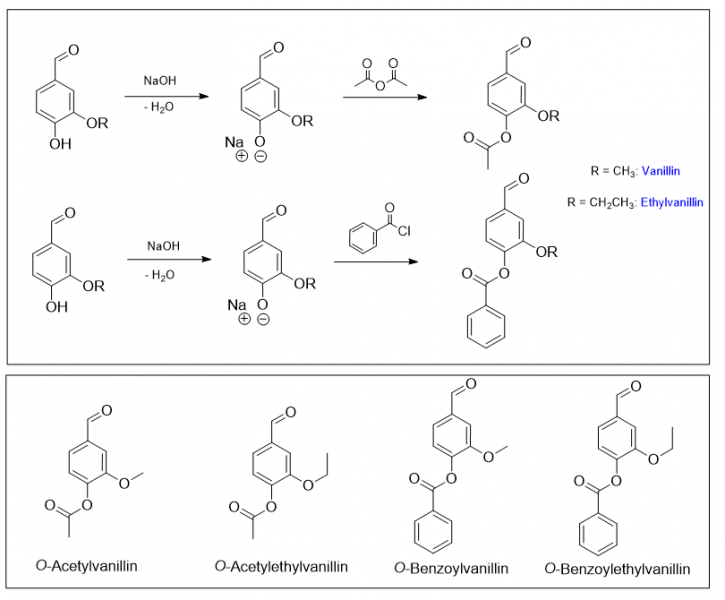
Im Zuge dieses Projekts soll die Synthese verschiedener Vanillinderivate gezeigt werden. Ein Schwerpunkt soll dabei auf den geruchlichen Eigenschaften dieser Verbindungen liegen. In diesem ersten Teil zielt die Mehrheit der durchgeführten Synthesen auf den Schutz der Phenol-Funktion der Vanilline ab. Durch die Veresterung dieser Gruppe mit Essigsäure oder Benzoesäure entstehen die jeweiligen Ester, wobei die Benzoat-Ester stabiler und schwerer zu spalten sind als die Acetat-Ester. Die dargestellten Verbindungen werden durch weitere Umwandlungen chemisch modifiziert, ohne dass die Hydroxyl-Gruppe dort zu Nebenreaktionen führen könnte. Schlussendlich wird der Ester wieder gespalten und das freie Phenol erhalten.
Unter den Begriff "vanilloid" fallen gemäß strenger Definition nur Substanzen, die den 4-OH-3-OMe-Benzylalkohol- oder Aldehyd als Strukturelement enthalten. Hier wird der Begriff allerdings etwas freier gebraucht, so werden im Zuge des Projekts auch Derivate des Anisaldehyds (4-Methoxybenzaldehyd) und weitere unter diesen Unterbegriff fallen.
Geräte:
Bechergläser, Erlenmeyerkolben, Rundkolben, Spatel, Tropftrichter, Pasteurpipetten, Vakuumpumpe, Magnetheizrührer, Destillationsapparatur, Eisbad, Vakuumfiltrationsanlage, Stativmaterial, Abzug, Zubehör für die Dünnschichtchromatographie.
Chemikalien:
Vanillin

Ethylvanillin

Natriumhydroxid

Essigsäureanhydrid



Benzoylchlorid


Diethylether


Isopropylalkohol



Iod



Natriumpersulfat



Brom



Cyclohexan




Ethylacetat


Kaliumiodid

Natriumsulfat
Natriumhydrogencarbonat
O-Acetylvanillin

O-Acetylethylvanillin

O-Benzoylvanillin

O-Benzoylethylvanillin

5-Bromvanillin

5-Iodvanillin

Hinweis: Benzoylchlorid und Brom sollten auf jeden Fall nur unter einem gut ziehenden Abzug verarbeitet werden. Das Einatmen von Bromdämpfen kann tödlich sein!
In fast allen Versuchen wird mit Aldehyden als Produkte gearbeitet, diese sind generell oxidationsempfindlich, auch wenn die individuelle Neigung hierzu unterschiedlich ist. Vor allem in Lösung (größere Oberfläche) sollten Aldehyde nicht länger als unbedingt nötig Luftkontakt haben, es sollte mit Schutzgas (Argon) gearbeitet werden. Generell hat sich aber im Zuge des Projekts gezeigt, dass die hier vorkommenden Aldehyde wohl eher weniger zur Oxidation neigen bzw. dies sehr langsam geschieht. Alternativ kann auch Stickstoff als Schutzgas verwendet werden.
Durchführung:
Vorbemerkung: Zur dünnschichtchromatographischen Untersuchung der Produkte wurden einige mg in ca. 1 ml Ethylacetat gelöst und ein Bruchteil dieser Lösung mit Hilfe einer Kapillare auf eine Silica F254 Kieselplatte aufgetragen. Als Elutionsmittel wurde Cyclohexan/Ethylacetat 3:2 verwendet. Die Detektion der Spots erfolgte durch UV-Licht mit 254 nm Wellenlänge.
O-Acetylvanillin:
In einem 500 ml Zweihals-Rundkolben werden 30,4 g (0,2 mol) reines Vanillin, zusammen mit 8,00 g (0,2 mol) NaOH vorgelegt. Es werden ca. 350 ml Wasser hinzugegeben und die Mischung solange unter magnetischem Rühren erhitzt, bis eine gelbe, klare Lösung entsteht. Diese lässt man wieder weitestgehend abkühlen, wobei keine Trübung oder Auskristallisieren von Natrium-vanillinphenolat stattfinden darf. Über einen Tropftrichter werden nun 20,4 g (0,2 mol) Essigsäureanhydrid über einen Zeitraum von ca. 10 Minuten eingetropft. Hierbei fällt normalerweise sofort ein weißer Niederschlag aus und die Mischung lässt sich unter Umständen nur noch schlecht rühren. In diesem Fall kann ein wenig Wasser zugegeben werden. Dann wird die Mischung fünf Stunden lang unter Argon-Atmosphäre gerührt, und der Niederschlag aus O-Acetylvanillin schließlich vakuumfiltriert. Er wird ausgiebig mit Wasser gewaschen und schließlich im Vakuum bei 25°C bis zur Gewichtskonstanz getrocknet. Dieses rohe Produkt enthält noch viel Vanillin und wird daher aus Isopropanol umkristallisiert (andere Lösungsmittel auch möglich).
Ausbeute: 21,0 g farblose Kristalle (54% d. Th.), ohne weitere Aufarbeitung der Mutterlauge.
Geruch: Leicht süßlich, mandelartig, cremig, minimal nach Essigsäure.

Ausgefallenes O-Acetylvanillin.

Ein kleiner Teil des trockenen, rohen Produkts.

Das umkristallisierte, fertige Produkt.

DC-Analyse: Unreines Produkt, gereinigtes Produkt, Vanillin.
O-Acetylethylvanillin:
In einem 500 ml Zweihals-Rundkolben werden - wie schon bei O-Acetylvanillin beschrieben - 16,6 g (0,1 mol) Ethylvanillin (3-Ethoxy-4-hydroxy-benzaldehyd) und 4,00 g (0,1 mol) NaOH in 200 ml Wasser in Lösung gebracht. In die abgekühlte, gelbe Lösung werden über 10-15 min. 12,8 g (0,125 mol) Essigsäureanhydrid (25% Überschuss) eingetropft. Intermediär kann ein weißer Niederschlag ausfallen, der sich aber wieder löst. Nach einigen Minuten färbt sich die Lösung rötlich. Die Mischung wird nun für fünf Stunden kräftig unter Argon-Atmosphäre gerührt. Danach wird sie für eine weitere Stunde bei ca. 60-80 °C gerührt, um die Hydrolyse des überschüssigen Acetanhydrids zu begünstigen. Nach dem Abkühlen liegt das Produkt als Emulsion in Wasser vor, nicht als Feststoff. Daher wird die Emulsion mit 2x 50 ml Diethylether im Scheidetrichter extrahiert. Die vereinigten Etherphasen werden zunächst mit wenig 5%iger NaOH gewaschen, dann zweimal mit ges. NaHCO3 und schließlich noch einmal mit dest. Wasser. Die gereinigte Etherphase wird über Natriumsulfat getrocknet und der Ether per Rotationsverdampfer oder Destillation abgezogen.
Vorsicht: Diethylether kann explosive Peroxide bilden. Er sollte nie bei großer Hitze rückstandsfrei abgedampft werden. Man kann Ether vorher auf das Vorhandensein von Peroxiden testen. Auch nutzungsbereite Teststreifen sind erhältlich.
Es bleibt schließlich eine ölige Flüssigkeit zurück, welche im Vakuum getrocknet wird (Raumtemperatur nicht überschreiten). Hierbei, oder spätestens beim Stehenlassen über Nacht, kristallisiert das O-Acetylethylvanillin zu schönen Kristallgebilden aus. Das Produkt enthält trotz des Waschens mit Natriumhydroxid-Lösung noch geringe Mengen Ethylvanillin. Durch den sehr niedrigen Schmelzpunkt lässt es sich jedoch schlecht umkristallisieren, weswegen auf eine weitere Reinigung verzichtet wurde. Für die DC-Analyse des Produkts, siehe bei O-Benzoylethylvanillin.
Ausbeute: 15,9 g (77% d.Th.) als wachsartige, gelbe Kristallmasse.
Geruch: Sehr angenehm süß, mandel-artig, weniger "scharf" als Ethylvanillin selbst.

Das Edukt: Ethylvanillin aus einem Parfum-Shop.

Rötliche Reaktionsmischung.

Das noch nicht auskristallisierte Produkt.

Auskristallisiertes Produkt.
O-Benzoylvanillin:
Es werden 7,60 g (0,05 mol) Vanillin und 2,00 g (0,05 mol) NaOH in 150 ml Wasser gelöst. Es erfolgt die langsame Zugabe von 7,00 g (0,05 mol) Benzoylchlorid (Abzug!) über einen Tropftrichter. Nach vollendeter Zugabe wird der Reaktionsansatz unter Argon gesetzt und 24 Stunden gerührt. Intermediär kann die Lösung rötlich werden. Nach einigen Stunden fällt das Produkt als Feststoff aus. Nach den genannten 24 Stunden wird das O-Benzoylvanilin vakuumfiltriert, mit viel Wasser und abschließend mit wenig Methanol gewaschen. Der leicht beige Feststoff wird vakuumgetrocknet. Falls das Produkt nicht ausfällt, wird die Mischung mit Ether extrahiert und dann wie bei O-Acetylethylvanilin weiter verfahren. Das Rohprodukt wird aus Isopropanol umkristallisiert, was jedoch leider zu hohen Verlusten in der Ausbeute führt.
Ausbeute: 3,50 g (28% d. Th.) farblose bis leicht beige Kristalle.
Geruch: Eigentümlicher, aber nicht unangenehmer Geruch.

Noch feuchtes Produkt nach der Vakuumfiltration.

Gereinigtes Produkt.

DC-Analyse des umkrist. Produkts: Links Produkt, rechts Vanillin.
O-Benzoylethylvanillin:
Man legt 8,30 g (0,05 mol) Ethylvanillin zusammen mit 2,00 g (0,05 mol) NaOH in 150 ml Wasser vor und gibt 7,00 g (0,05 mol) Benzoylchlorid langsam zu. Die Mischung wird über Nacht (24 Stunden) unter Argon gerührt. Dabei fällt ein beiger Niederschlag aus, welcher abfiltriert und mit viel Wasser und abschließend Methanol gewaschen wird. Schließlich wird er bei maximal 40°C Wasserbad-Temperatur im Vakuum getrocknet. Falls die Verbindung nicht fest ausfällt, verfährt man nach dem schon beschriebenen Ether-Extraktionsverfahren. Das Rohprodukt wird aus Isopropanol umkristallisiert.
Ausbeute: 3,00 g ( 22% d. Th.) beige Kristalle.
Geruch: Eigenartiger, schwach-süßer Geruch.

Ausgefallenes O-Benzoylethylvanillin.

Noch zu trocknendes Produkt.

Umkristallisiertes Produkt.

DC-Analyse von O-Acetylethylvanillin und O-Benzoylethylvanillin: Et-Van, OAc-Et-Van, OBz-Et-Van.
5-Bromvanillin:
Es wird eine Lösung von 15,2 g (0,1 mol) Vanillin in 100 ml Methanol bereitet, welche anschließend auf 0°C im Eisbad gekühlt wird. Der Kolben wird dann mit Argon geflutet. Über einen Zeitraum von 20 min. werden vorsichtig und unter kräftigem Rühren 18,0 g (0,113 mol) elementares Brom eingetropft (Vorsicht: Hochgiftig!). Nach der Zugabe wird eine Stunde bei Raumtemperatur gerührt. Die Mischung wird dann wieder ins Eisbad gestellt und mit 50 ml Wasser versetzt. Der entstandene Niederschlag wird vakuumfiltriert, mit 2x 50 ml Wasser und abschließend 1x mit 50 ml MeOH/Wasser 7:3 gewaschen. Das feuchte Produkt wird bei leicht erhöhter Temperatur (ca. 50°C) im Vakuum getrocknet. Für DC-Analyse des Produkts, siehe 5-Iodvanillin unten.
Ausbeute: 22,8 g (99% d. Th.) leicht gelbliches Pulver.
Geruch: Nahezu geruchslos, eventuell leicht muffig. Dient als Intermediat.

Das abgewogene Brom.

Während der Zugabe des Broms.

Ausgefallenes Produkt.

Vakuumtrocknung des Produkts.
5-Iodvanillin:
In einem 250 ml Rundkolben werden 10,0 g (0,06 mol) Kaliumiodid, 12,6 g (0,05 mol) Iod und 5,00 g (0,06 mol) Natriumhydrogencarbonat in 200 ml Wasser gelöst. Dann erfolgt die direkte Zugabe von 7,60 g (0,05 mol) Vanillin. Die Mischung wird fünf Stunden unter Argon gerührt und schließlich über Nacht stehen gelassen. Der beige-braune Niederschlag wird abfiltriert, mit Wasser gewaschen und in leicht getrockneter Form aus Ethanol/Isopropanol 2:1 umkristallisiert. Hierbei entstehen sehr schöne fluffige Kristallnadeln. Das Einengen der Mutterlauge beim Umkristallisieren erhöht die Ausbeute um ca. 15%. Das 5-Iodvanillin wird im Vakuum getrocknet.
Hinweis: Das wässrige Filtrat enthält noch viel Iodid. Durch Zugabe von entsprechend Natriumperoxodisulfat lässt sich dieses als Iod ausfällen und somit die Hälfte des eingesetzten Iods zurückgewinnen.
Ausbeute: 8,84 g hellgelber Kristallnadeln (65% d.Th.).
Geruch: Die Substanz ist geruchslos und dient als Intermediat.

Nach dem Stehenlassen abgesetztes Produkt.

Aus der Alkohol-Mischung umkristallisiert.

Trockenes 5-Iodvanillin.

DC-Analyse, von links nach rechts: Vanillin, 5-Br-Vanillin, 5-I-Vanillin.
Entsorgung:
Die Substanzen werden in den anorganischen bzw. organischen Müll gegeben und einem Entsorgungsunternehmen zugeführt. Harmlose Reste können über den Abfluss entsorgt werden. Vor allem übriges Brom und Iod müssen mit Reduktionsmitteln wie Thiosulfat oder Sulfit entstört werden.
Erklärungen:
Die O-Acetyl- und O-Benzoylverbindungen entstehen durch Veresterung der Phenolfunktion. Um das Gleichgewicht auf die Seite der Produkte zu verschieben, nutzt man Carbonylverbindungen, die wesentlich reaktiver sind als die Carbonsäuren, nämlich Anhydride und Carbonsäurechloride. Während sich die phenolischen Edukte in Natronlauge unter Deprotonierung lösen (ihre Reaktivität wird durch die negative Ladung auch erhöht), ist dies bei den Estern selbstverständlich nicht mehr möglich. Die Produkte fallen daher aus der wässrigen Lösung aus und können abfiltriert werden. Die Veresterung kann auch (vermutlich auch mit besseren Ausbeuten und Umsatz) in organischen Lösungsmitteln durchgeführt werden.
Vanillin und seine Derivate können in Position 5 bromiert und iodiert werden, da dort eine hohe Elektronendichte vorherrscht. Mechanismus: Elektrophile aromatische Substitution (EAS). Im nachfolgenden Mechanismus sei die Bromierung als Beispiel herangezogen. Die Iodierung wurde anders als die Bromierung in wässriger Lösung durchgeführt. Das Hinzufügen von Kaliumiodid führt zur Bildung der Triiodid-Spezies mit einer gewissen Wasserlöslichkeit.

Im Fazit konnten jeweils zwei verschiedene Ester von Vanillin und Ethylvanillin in reiner Form (abgesehen vom nicht weiter aufgearbeiteten O-Acetylethylvanillin) gewonnen werden. Besonders O-Acetylvanillin steht mir nun in ausreichender Menge zur Verfügung, um weitere Synthesen damit zu planen und durchzuführen. Eines von mehreren target molecules soll der Vanillylbutylether sein, der aufgrund seines Geruchs und seiner leichten Schärfe Verwendung findet.

