In diesem Versuch wird beschrieben, wie man die Qualitatät eines Oberflächenwassers, anhand seiner Faulfähigkeit bestimmen bzw. bewerten kann.
Geräte:
Becherglas 100ml, Spatel, Chemikalienflasche 1000ml, Maßkolben 1000ml, Chemikalienflasche bzw. Steilbrustflasche Klarglas mit Schliff bzw. Schraubkappe, Präzisionswaage (Ablesbarkeit 0,000g),
Wasserfester Stift und Etiketten, Wärmeschrank, Latexhandschuhe, Cellstoff-Tücher, Injektionsspritze (2ml), Trichter
Chemikalien:
Methylenblau krist. oder plv.

Dest. Wasser
Wasserprobe verschiedener Herkunft
z.B. Flusswasser, Teichwasser, Wasser aus Tümpeln
Hinweise:
Bitte beachtet das Methylenblau ein extrem intensiver Farbstoff ist. Ich empfehle euch auf jeden Fall gleich eine große Menge an Methylenblau-Lösung anzusetzen.
So ist das Risiko geringer irgend wann mal etwas zu verschütten oder sich seine Waage zu versauen. Die Lösung sollte fest verschlossen, in einer
stabilen Kunststoffflasche aufbewahrt werden.
Durchführung:
Zuerst legt ihr am besten den ganzen Arbeitsplatz mit Zeitungspapier aus. Legt euch alle Materialien übersichtlich zurecht und fangt dann an die Substanz (Methylenblau) abzuwiegen.
Um eine 0,05%ige Methylenblau-Lösung herzustellen, müsst ihr 0,5g Methylenblau einwiegen. Diese Masse bezieht sich auf 1 Liter.
Jetzt nehmt das Becherglas und füllt es bis zur Hälfte mit Dest. Wasser. Gebt die leicht verrührte Lösung über den Trichter in den Maßkolben und wiederholt den Vorgang so lange, bis sich das gesamte Methylenblau
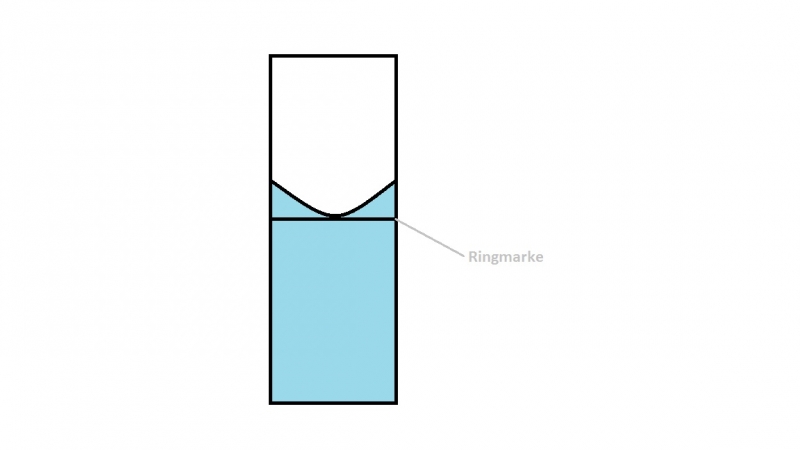
im Maßkolben befindet. Gebt weiter, unter kreisenden Bewegungen, Dest. Wasser in den Maßkolben, bis kurz vor die Ringmarke und stellt dann mit etwas Gefühl den Meniskus ein. Bitte beachtet, das bei dunklen Flüssigkeiten
der Meniskus gesondert eingestellt wird (seht dazu Bild 1 und 2). Ist der Meniskus eingestellt, wird der Maßkolben verschlossen und die darin enthaltene Lösung durch kräftige Auf- und Ab-Bewegungen des Kolbens durchmischt
(Bitte den Stopfen gut festhalten). Nun werden, je nach Anzahl an Wasserproben, die 100ml Flaschen bereitgestellt und mit jeweils 1ml Methylenblau-Lösung beschickt. Jetzt gibt man so lange die jeweilige Wasserprobe hinzu,
bis die Flasche komplett gefüllt ist. Je weniger Luft sich in der Flasche befindet, um so genauer wird am ende das Ergebnis. Achtet bitte darauf das die Flaschen fest verschlossen sind. Jetzt wird jede Flasche solange geschüttelt, bis die
Lösung darin einheitlich blau erscheint. Denkt bitte daran die Flaschen zu beschriften. Am besten mit dem Datum des jeweiligen Tages und der Art der Probe, bzw. Ort. Stellt die Flaschen nun an einem warmen Ort oder wenn vorhanden in einem Brutschrank und kontrolliert am ersten Tag stündlich, ab dem 2. bis zum 5. Tag, täglich, auf eine Entfärbung.
Tritt eine Entfärbung ein, so notiert das Datum und errechnet daraus die Tage bis zur entfärbung. Ist am 5. Tag immer noch keine Entfärbung eingetreten, kann man daraus schließen, dass das Wasser gering mit organisch-faulfähigen Stoffen belstet ist.
Die Beurteilung erfolgt dabei am ersten Tag in Stunden bis zur Entfärbung (z.B. nach 4 Stunden entfärbt: 4he) vom 2. bis 4. Tag in Tagen (z.B. nach 3 Tagen entfärbt: 3de). Ist die Lösung am 5. Tag immer noch nicht entfärbt
wird die Probe als n.e. (nicht entfärbt) beurteilt.
Entsorgung:
Die bei der Betimmung anfallende Lösung (entfärbt oder nicht entfärbt), wird stark verdünnt dem Abwasser zugeführt.
Erklärung:
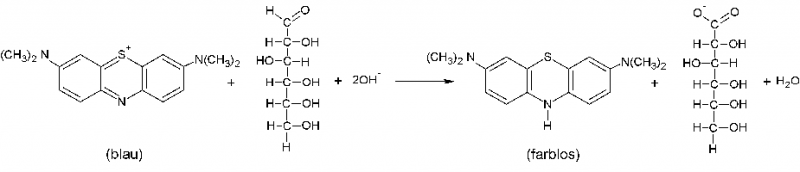
Methylenblau ist ein Redoxindikator. Dieser entfärbt sich unter absoluten Luftabschluss in dem Maße, in dem anaerobe Vorgänge ablaufen.
Je stärker diese, um so stärker ist auch die Entfärbung des Methylenblau.
Bilder:
Meniskus bei hellen Flüssigkeiten
Bild 1.

Meniskus bei dunklen Flüssigkeiten
Bild 2.

Hier das Methylenblau als Feststoff und als Lösung
Bild 3.

Hier die Flaschen mit Probelösungen nach 5 Tagen
Bild 4.