Hier soll die Wellenzahl einer IR-Schwingung berechnet werden. Dazu erfolgt zuerst eine Modellierung und dann die eigentliche Berechnung.
Modellierung
Das IR-Spektrum kann grundsätzlich in 2 Bereiche aufgeteilt werden. Bis ca. 1600 cm-1 handelt es sich um sogenannte Deformationsschwingungen, das Molekül ändert also seine Form, wobei es viele Möglichkeiten gibt über welche man sich in der Literatur ausgiebig informieren kann.
Über 1600 cm-1 beginnen Valenzschwingungen, d.h. die Bindungen schwingen wie Federn, wobei allerdings nur asymmetrische Valenzschwingungen IR-aktiv sind, da sich nur in diesem Fall das Dipolmoment ändert. Andere Schwingungen sind Raman-aktiv.
Wie bereits gesagt schwingen die einzelnen Atome/funktionellen Gruppen an der Bindung, welche als Feder abstrahiert werden kann. Daher folgt diese Schwingung dem Hookeschen Gesetz für oszillierende Schwingungen. Allgemein gilt dabei, dass die Auslenkung zur Kraft proportional ist. In atomarer Ebene gibt es hier die Kraftkonstante als Maß für die Bindungsstärke.
Für die Schwingungsfrequenz gilt nach einigen Umformungen :

v ist die Schwingungsfrequenz
k = Kraftkonstante in N/cm

m1 entspricht der Masse auf der einen Seite, m2 auf der anderen Seite der Bindung. Um die Modellierung einfach zu halten, soll die OH-Schwingung im Methanol berechnet werden.
Berechnung
Zuerst muss zur Kontrolle der Berechnung ein IR-Spektrum von Methanol aufgenommen werden (FT-ATR, 4 Scans, 500-3400 cm-1).

Jetzt setzt man in die Formel alle gegebenen Variablen ein.
Um die reduzierte Masse zu berechnen, muss erst das Atomgewicht in Kilogramm umgerechnet werden. Dazu teilt man die Massen in u durch 1000 und dann das Ergebnis durch die Avogadrokonstante.
Die Kraftkonstante beträgt 501,49 N/cm, wobei hier eine Angabe in kg*s² zweckmäßiger ist.
Nach Einsetzen erhält man eine Frequenz von ~ 88,5 THz. Nun muss man daraus noch die Wellenlänge berechnen. Es gilt λ = c/v, man erhält die Wellenlänge in m, welche mit 100 multipliziert wird. Der reziproke Wert entspricht dann der Wellenzahl von 2952,77 cm-1.
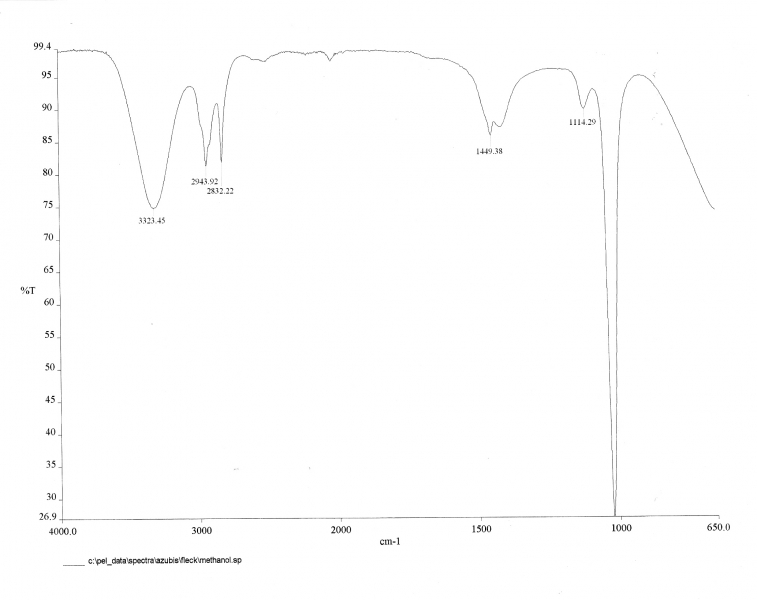
IR-Spektrum von absolutem Methanol p.a. ; die Aufnahme erfolgte im BfArM mit Dank an Dr. Jochen Norwig