Geräte:
Erlenmeyerkolben mit Stopfen 1 l oder Getränkeflasche 1 l ausgewaschen
Chemikalien:
Methylenblau
Natriumhydroxid
Glucose
Durchführung:
Man füllt die Flasche mit 900ml Wasser und löst 10g Natriumhydroxid darin. Wenn die Flasche zu heiß wird, kühlen. Wenn das ganze Natriumhydroxid gelöst ist, gibt man 80g Glucose und 0,05g Methylenblau dazu. Man schließt die Flasche und schüttelt bis alles gelöst ist. Wenn man die Flasche geschlossen stehen lässt, entfärbt sich die Flüssigkeit langsam. Schüttelt man sie wieder, kommt die Blaufärbung wieder. Dies kann man so oft machen, wie man will.
Erklärung:
Glucose reduziert Methylenblau zu Leukomethylenblau, wobei die Glucose zu Gluconsäure oxidiert wird. Das Leukomethylenblau wird über den Luftsauerstoff in der Flasche wieder zu Methylenblau oxidiert.
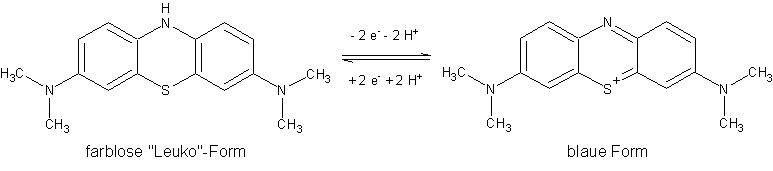
Entsorgung:
Die Lösung wird neutralisiert und dann in den Ausguss gegeben.
Bilder:


Video:






