(TsOH)
para-Toluensulfonsäure ist ein wichtiger Katalysator in der synthetischen Chemie für säurekatalysierte Kondensationsreaktionen und Eliminierungen, etwa für die Herstellung von Alkenen, Estern, Acetalen (Einführung einer Schutzgruppe) oder Enaminen. Seine Eignung ergibt sich aus der großen Säurestärke bei gleichzeitig günstiger Handhabung. Wie Schwefelsäure ist sie sehr hygroskopisch, das hier hergestellte Präparat sollte in eine Ampulle eingeschmolzen oder in einer Flasche mit dicht schließendem Gebinde aufbewahrt werden. Ihre Ester, die Tosylate, sind dahingehend interessant, dass sie sowohl als Alkylantien als auch dazu genutzt werden können, Hydroxylgruppen zu besseren Abgangsgruppen umzufunktionalisieren. Für ihre Herstellung eignet sich jedoch Tosylchlorid besser.
Geräte:
Rundkolben, Wasserabscheider, Dimrothkühler, Trockenrohr, Heizpilz, Magnetrührer, Geräte für die Entwicklung von Chlorwasserstoff, Standardequipment
Chemikalien:
Toluen


Schwefelsäure
Natriumchlorid
4-Toluensulfonsäure

Hinweis:
Vorsicht im Umgang mit siedender Säuremischung.
Durchführung:
Es wird eine Apparatur zur Wasserabscheidung aufgebaut und mit einem Trockenrohr vor dem Eindringen von Luftfeuchtigkeit geschützt. In den Reaktionskolben wurden 80 ml trockenes Toluen und 13,3 ml konzentrierte Schwefelsäure gegeben und mit der Erwärmung begonnen. Die anfängliche Phasenbildung geht zurück (Anm. 1) und schließlich gerät der Ansatz ins Sieden, wobei das Toluen-Wasser-Azeotrop (bp.: 80 °C) übergeht. Das übergehende Destillat wird abgetrennt und die Wassermenge zur Kontrolle des Reaktionsfortschritts bestimmt. Ab einer Dauer von 3 h (Lit.: 5 h) geht kein Wasser mehr über, sodass die Destillation nicht mehr fortgeführt werden sollte. Der erkaltete Ansatz sollte im Eisbad temperiert werden, bevor man langsam 4,5 ml Wasser in den Kolben tropft (Anm. 2), wobei sich Kristalle des Sulfonsäurehydrats bilden. Diese werden über eine Glas(!)fritte scharf abgesaugt und in wenig heißem Wasser gelöst. Ist diese Mutterlauge gefärbt, so erfolgt die Abtrennung von Verunreinigungen durch Filtern über Aktivkohle in der Hitze. Diese gesättigt Lösung wird, um Kristallisation einzuleiten, mit HCl saturiert, dazu wird zweckmäßig ein Trockenrohr als Gaseinlasszylinder verwendet, um Verstopfungen durch Produktkristalle zu vermeiden. Die rein weißen Kristalle müssen nun wiederum scharf vakuumfiltriert und über Hydroxid getrocknet werden (Anm. 3).
Ausbeute: 17,3g (40,1% d.Th.) (Lit.: 40%)
TsOH bildet weiße Tafeln oder Nadeln, die stark hygroskopisch sind und mitunter metallene Geräteteile schädigen können.
Entsorgung:
Die flüssigen Abfälle gelangen zu den halogenfreien, organischen Abfällen.
Erklärung:
Für Aromaten mäßiger Reaktivität wie Toluen genügt bereits heiße konzentriere Schwefelsäure zur Führung einer Sulfonierung. Das angreifende Elektrophil ist das HSO3+-Kation, welches mit dem Toluen eine elektrophile aromatische Substitution eingeht (Die Methylgruppe dirigiert in ortho/para-Position). Diese Reaktion ist reversibel, dabei ist der Zerfall der Sulfonsäure bei erhöhter Temperatur begünstigt (Nutzung dieses Effekts zur ipso-Substitution für die Nitrierung von Phenolen), weswegen das Reaktionswasser destillativ abgezogen werden muss. Das elektrophile Teilchen ist planar und relativ groß, weshalb die Substitution in para-Stellung begünstigt ist.
Mechanismus:
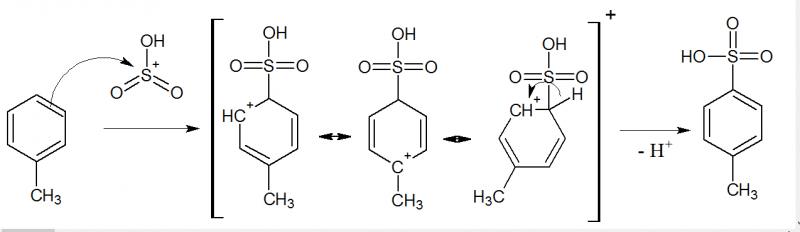
Bilder:

Apparatur zur Wasserabscheidung mit Toluen

Das Rohprodukt, welchem noch größere Mengen Toluen und o-Isomer anhaften

Das rekristallisierte Produkt
Quellen / Literatur:
Organikum 22. Auflage, Weinheim, 2004, p. 366