Ich kann mich da Xyrofl nur anschließen, die Cyclopropane sind ein wenig spezieller, aber nicht im Sinne
ungeheurer Reaktivität, sondern eher
unerwarteter Reaktivität. Natürlich sind die Verbindungen recht reaktiv, aber weniger als man auf den ersten Blick vermuten würde. Sehr deutlich zeigt sich das auch in den Bindungslängen, da diese kürzer sind als bei Alkanen üblich. Ein ähnliches Phänomen hat man ja auch bei den C-C-Bindungen im Benzol beobachtet, deren Bindungslängen liegen zwischen typischen Alkan- und Alkenbindungslängen. Bei den Cyclopropanen ist es ähnlich, wobei der veränderte Bindungscharakter (erhöhter π-Charakter ) nicht durch Delokalisation von Elektronen wie bei Aromaten zustande kommt. Durch den niedrigen Bindungswinkel wird keine typische sp
3-Orbitalüberlappung gewährleistet und die Bindung "biegt" sich aus der Kern-Kern-Achse, weshalb man auch von
Bananenbindungen oder
Bent bonds spricht (vergleichbares kennt man auch von den Bindungszuständen im Diboran).
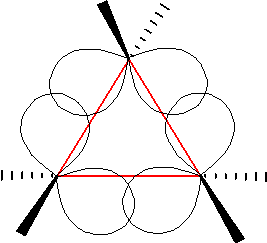
[Wiki]
Für das Cyclopropan wurde außerdem eine andere Theorie entwickelt, welche versucht, typische Reaktivitäten des Cyclopropans zu erklären. Wer mehr dazu wissen möchte kann sich mal das
Walsh-Modell anschauen.
Ein schönes Beispiel stellt hier das
Bracken-Dienone 3 dar. Der ein oder andere hat (auf dem Forentreffen) bestimmt schon ein wenig vom
Ptaquilosid 1 (aus
Pteridium aquilinum) mitbekommen, welches nach formaler Eliminierung von Glucose unter biologischen Bedingungen quasi "scharfgeschaltet" wird. Durch Hydrolyse und anschließende Deprotonierung in 9-Position (wobei der Austritt von OH
- hier durch die
syn-Stellung beider Gruppen und der erhaltenen Konjugation begünstigt ist) liegt nun ein δ-Cyclopropyldienon vor (ein ungewöhnlicher Michael-Akzeptor). Durch den erhöhten π-Charakter ist der Cyclopropanring als konjugiert zu betrachten und wird durch Nucleophile (z.B. DNA) angegriffen (oder greift diese elektrophil an), wobei es gleichzeitig unter Austritt eines weiteren OH
--Ions zu einer vollständigen Aromatisierung des Sechsrings kommt.
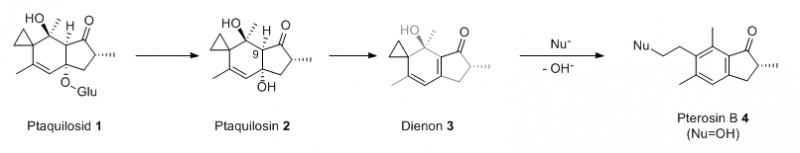
Das so erhaltene Trimethylindanon
4 ist besonders stabil und im Falle von DNA als Nucleophil nun kovalent an diese gebunden, was es zu einem potenten Carcinogen des Adlerfarns macht. Es gab auch Versuche sich diese Reaktivität der Illudine (welche sich vom Illudan-Gerüst ableiten, Ptaquilosid ist als Norsesquiterpenglycosid des Illudan-Typs zu betrachten) für die Krebstherapie zu Nutze zu machen, dem aber zumeist die Toxizität der Verbindungen gegenüber steht.

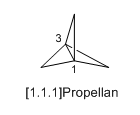
Da wir gerade bei Dreiringsystemen sind, sollte das [1.1.1]Propellan nicht ungenannt bleiben. Anfangs dachte man, dass man es nicht möglich sei den einfachsten Vertreter der Propellane zu synthetisieren, da dieser zu reaktiv und instabil sei, jedoch konnte es später synthetisiert werden und ist bei Raumtemperatur stabil. Hierbei ist die tetraedrische Geometrie am Kohlenstoff invertiert und die C
1-C
3-Bindung mit 1,605 Å nur etwas länger als für ungespanntes Ethen und ist weniger energetisch als der biradikalische Zustand. Für die meisten Reaktion kann diese Bindung als doppelbindungs-artig betrachtet werden und addiert zum Beispiel sehr leicht Iod. Diese Betrachtungsweise ist aber nicht perfekt, da hier auch Angriffe von Nucleophilen erfolgen.