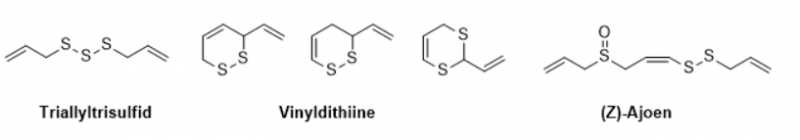
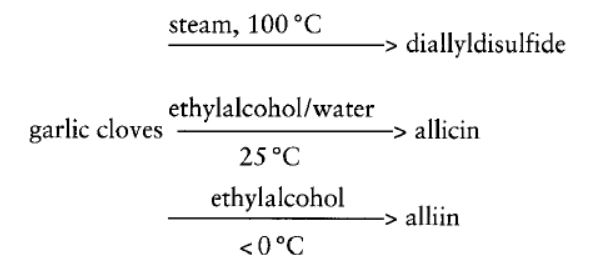
Knoblauch (Allium sativum) ist eine weltweit verbreitete Heil- und Gewürzpflanze, welche sich durch ihren charakteristischen Geruch auszeichnet. Interessant ist jedoch die Tatsache, dass die eigentlichen Geruchsstoffe im Knoblauch selbst nicht vorkommen, sondern erst nach dem Zerstören der Knollen gebildet werden. Die im Zytoplasma gespeicherte, schwefelhaltige und geruchlose Aminosäure Alliin bildet dabei das erste Glied einer Reaktionskette aus der sich letztendlich die intensiv riechenden Verbindungen bilden, sobald die Knolle beschädigt wird und das in den Vakuolen enthaltene Enzym Alliinase mit dem Alliin in Kontakt kommt. Das dabei entstehende Thiosulfinat Allicin, welches ebenfalls geruchlos ist, ist synthetisch leicht zugänglich, jedoch sehr instabil, so dass es bereits nach wenigen Stunden oder Tagen weitgehend zersetzt ist. Hier wird die Synthese des Allicin über Diallyldisulfid im Halbmikromaßstab beschrieben, jedoch auf die Aufreinigung verzichtet, sodass nur ein sehr unreines Produkt erhalten wird, was - je nach Temperatur - weiter in die aktiven Riechstoffe des Knoblauchs zerfällt.
Geräte:
50 mL Rundkolben, diverse Glasgeräte, Rückflusskühler, Scheidetrichter, Glasfritte, Magnetheizrührer, Rotationsverdampfer
Chemikalien:
Allylbromid



Thioharnstoff


Triethylamin


Tetrachlormethan


Glycerol, wasserfrei
Natriumsulfat, wasserfrei
Hexan



Ethylacetat
3-Chlorperoxobenzoesäure (CBPA)


Natriumhydrogencarbonat
Diethylether
Dichlormethan
Diallyldisulfid

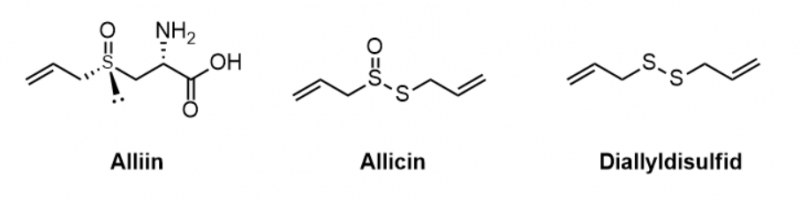
Aliicin
Hinweis: Die dargestellten Verbindungen sind sehr geruchsintensiv. Das hergestellte Produkt sollte trotz des angenehmen Aromas keinesfalls für Lebensmittel verwendet werden.
Durchführung:
Diallyldisulfid
In einem 50 mL Rundkolben werden 1,9 g Thioharnstoff, 4,65 mL Triethylamin, 3,9 mL Tetrachlormethan in 20 mL wasserfreiem Glycerin vorgelegt und 1 mL Wasser zugegeben. Unter Rühren werden 1,75 mL Allylbromid zugesetzt und die Mischung für 12 h bei 50 °C gerührt. Nach der Reaktionszeit werden 10 mL Wasser zugegeben, die Lösung mit Ethylacetat extrahiert (4x30 mL) und die organische Phase mit Natriumsulfat getrocknet. Der Rückstand wird auf ein Kieselgelpad gegeben, mit Hexan eluiert und anschließend das Lösungsmittel unter vermindertem Druck entfernt.
Ausbeute: 155 mg (10 % d.Th., Literatur: 94 %)
Allicin
152 mg Diallyldisulfid werden in 5 mL Dichlormethan gelöst und unter Rühren eine Lösung von 240 mg mCPBA in 4 mL DCM gelöst langsam unter Rühren zugesetzt. Die Lösung wird anschließend für eine Stunde auf 40 °C erwärmt und nach dem Abkühlen mit 5%-iger Natriumhydrogencarbonatlösung (4x5 mL) und Wasser (4x5 mL) gewaschen. Das Waschwasser wird mit Diethylether extrahiert und die vereinigten organischen Phasen über Natriumsulfat getrocknet. Am Rotationsverdampfer (Badtemperatur: 25 °C) wird das Lösungsmittel unter vermindetem Druck abdestilliert und es verbleibt ein gelbes, aliicinhaltiges Öl.
Ausbeute: 117 mg
Entsorgung:
Die Lösungsmittel sollten nicht recycelt sondern in die entsprechenden Abfälle gegeben werden, das Produkt wird über die halogenfreien Lösungsmittelabfälle entsorgt.
Erklärung:
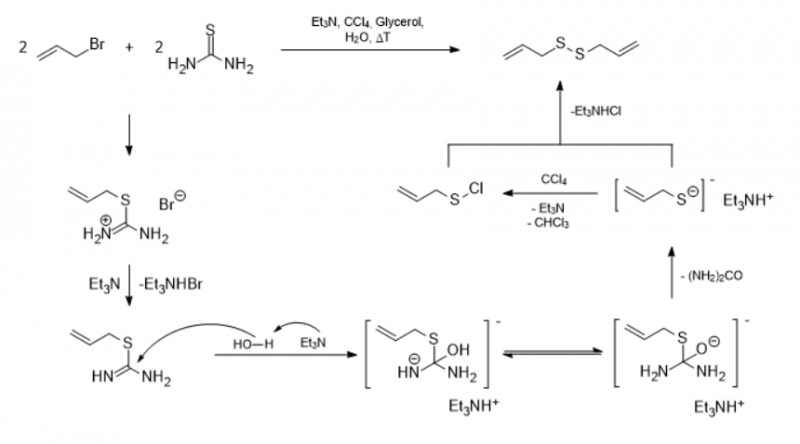
Die Bildung des Disulfids erfolgt über das Allylthiolat nach Schwefeltransfer durch Thioharnstoff und Deprotonierung mittels Triethylamin. Das Tetrachlormethan stellt das notwendige Chloratom zur Verfügung und verbleibt als Trichlormethan in der Lösung. Der finale Schritt ist die Reaktion des Thiolats mit dem gebildeten Sulfenylchlorid, welche das Disulfid bilden. Ein denkbares Nebenprodukt wäre Diallylsulfid, welches entsteht, wenn nicht umgesetztes Allylbromid mit dem gebildeten Thioat reagiert.
- wird ergänzt -
Bilder:

Reaktionslösung vor dem Erwärmen

Fortgeschrittene Reaktion

Nach beendeter Reaktion

Reaktionslösung nach der Oxidation, die blaue Fluoreszenz rührt von Verunreinigungen des Diallyldisulfids her

Trocknendes Extrakt

Allicinhaltiges Produkt