Geräte:
Erlenmeyerkolben 50 mL, Spatel, Pipette
Chemikalien:
Dichlormethan
Oxalylchlorid
9,10-Diphenylanthracen
Rubren
9,10-Bis(phenylethinyl)anthracen

Hinweis:
Oxalylchlorid reagiert heftig mit Wasser! Weiterhin baut sich in der Vorratsflasche schon nach kurzer Zeit Druck durch durch Zerfall entstehendes, sehr giftiges Phosgen auf! Abzug!
Durchführung:
In einem Erlenmeyerkolben werden 50 mg 9,10-Diphenylanthracen oder ein anderer geeigneter Farbstoff sowie 1 mL Oxalylchlorid unter Umschwenken in 20 mL Dichlormethan gelöst. Man gibt 1 mL 30%iges Wasserstoffperoxid hinzu, wobei bereits ein bei Umgebungslicht sichtbares Aufleuchten stattfindet. Man dunkelt den Raum ab und schwenkt um.
Entsorgung:
Die Lösung wird zu den halogenhaltigen organischen Lösemittelabfällen gegeben. Die Farbstoffe können zu den organischen Abfällen gegeben werden.
Erklärung:
Das Oxalylchlorid reagiert mit Wasserstoffperoxid zu 1,2-Dioxetandion:

Dieses zerfällt zu elektronisch angeregtem Kohlenstoffdioxid, welches wiederum den zugesetzten Fluoreszenzfarbstoff anregt, der daraufhin unter Emission eines Photons in seinen Grundzustand zurückkehrt.
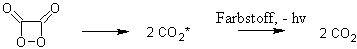
Bild:

Chemilumineszenz mit 9,10-Diphenylanthracen