5 g Vanillin und 1 g L-(+)-Ascorbinsäure mit einem Reinheitsgrad von jeweils 99,5% (Lebensmittelqualität) wurden in einem 100 ml Becherglas aus Borosilikatglas mit einem Glasstab grob vermischt und dann auf einem magnetischem Heizrührer und Einstich-Temperaturfühler unter ständigem Rühren auf 100 ºC unter dem Abzug erhitzt. Es zeigte sich, dass sich die Ascorbinsäure bei dieser Tempertur nicht in dem verflüssigten Vanillin lösen lässt. Unter ständigem Rühren wurde die Tempertur der Vanillinschmelze dann auf 130 ºC angehoben. Nach etwa 15 Minuten war die Ascorbinsäure komplett in Lösung gegangen, verbunden mit einem grünen Farbumschlag der Lösung.

Abb. 1 Grünfärbung der Vanillin-Ascorbinsäure-Lösung. Am Becherrand ist re-sublimiertes Vanillin zu erkennen
Warum Farbumschlag nach Grün?
Die erste Vermutung war, dass die Ascorbinsäure die Edelstahlummantelung des sich in der Lösung befindlichen Einstich-Temperaturfühlers angegriffen und so grüngefarbte Nickelsalze in die Vanillinschmelze geraten waren. Um dies auszuschließen, wurde statt des magnetischen Heizrührers ein Siliconölbad mit außenliegendem Thermostat verwendet und das Vanillin und die Ascorbinsäure ohne die Hilfe eines Edelstahllöffels oder –spatels in ein frisch gereinigtes und getrochnetes Becherglas gegeben und mit einem frisch gereinigten und getrochneten Glasstab gerührt. Aber auch hier zeigte sich das gleiche Phänomen: Sobald die Ascorbinsäure bei 130 ºC anfing, in Lösung zu gehen, schlug die blaßgelbliche Vanillinschmelze allmählich nach Grün um. Die Grünfärbung wurde umso intensiver, je langer die Lösung auf 130 ºC gehalten und gerührt wurde.
Um auszuschließen, dass der Farbumschlag auch ohne Zugabe von Ascorbinsäure stattfindet, wurde Vanillin unter Rühren für 20 Minuten auf 130 ºC erhitzt. Es wurde kein Farbumschlag nach Grün festgestellt. Nach Abkühlung kristallisierte das Vanillin sofort fischschuppenförmig aus.
Es wurde ebenfalls festgestellt, dass sich Ascorbinsäure bei Zugabe zu bereits länger erhitztem Vanllin schlechter löst und dann auch kein Farbumschlag nach Grün stattfindet.
Wird Ascorbinsäure und Vanillin in 70%igem Methanol gelöst und das Lösungsmittel dann eingedampft, färbt sich die Schmelze bei 130 ºC nicht grün sondern orange-braun. Dies kann daran liegen, dass die Ascorbinsäure bedingt durch den Wasseranteil im Lösungsmittel bereits zur Dehydroascorbinsäure oxidiert wurde.

Abb. 2 Orange-braun gefärbte Schmelze nach dem Verdampfen des Lösungsmittels
Metastabilität der Lösung
Die auf Raumtemperatur abgekühlte Vanillin-Ascorbinsäure-Lösung wies eine honigartige, einphasige und transparente Struktur ohne den typischen Geruch von Vanille auf. Diese behielt die Lösung etwa eine Stunde bei, bis plötzlich Kristallisation einsetzte. Innerhalb weniger Minuten war die komplette Lösung von langnadeligen Kristallen durchzetzt, auch der Geruch von Vanille nahm wieder merklich zu. Eine Erwärmung war nicht festzustellen.

Abb. 3 Kristallisation der zunächst klaren Lösung setzt ein
Der Kristallisation kann beschleunigt werden, indem man etwas Vanillinstaub auf die Oberfläche gibt. Um die winzigen Impfkristalle wachsen dann innerhalb von Minuten weitaus größere.
Auch bei Zugabe zu von Ascorbinsäure zu bereits länger erhitztem Vanillin ohne Farbumschlag nach Grün wies die Lösung eine honigartige, einphasige und transparente Struktur ohne den typischen Geruch von Vanille auf.
Es geht auch einfacher
In ein Reagenzglas aus Borosilikatglas wird eine Messerspitze Ascorbinsäure und eine Messerspitze Vanillin gegeben und gemischt, dann in ein Stativ eingespannt oder mit Reagenzglashalter vorsichtig über sehr kleiner Spiritusflamme erhitzt. Die Schmelze verfärbt sich in wenigen Sekunden dunkelgrün.

Abb. 4 Experiment mit einfachen Mitteln
Erklärung
Die Schmelze aus Vanillin und Ascorbinsäure ist eine Art Glas, d. h. sie ist nicht kristallin sondern amorph (Glas wird oft auch als unterkühlte Schmelze oder sogar als eine Flüssigkeit mit sehr hoher Viskosität bezeichnet). Die Kristallinitat des Vanillins wird durch den zugesetzten Fremdstoff Ascorbinsäure (oder deren Abbauprodukte) so weit zerstört, dass eine Transparenz resultiert. Ascorbinsäure-Moleküle besetzen statistisch Positionen, die ursprünglich in der Vanillin-Kristallstruktur von Vanillin- Molekülen besetzt waren. Dieser Vorgang ist jedoch nicht statischer sondern dynamischer Natur. Nach und nach erobern sich die Vanillin- Moleküle die Positionen zurück, wodurch es zur Auskristallisierung kommt.
Eine Möglichkeit für die Grünfärbung ist, dass Abbauprodukte der Ascorbinsäure wie Furfural mit der Phenolkomponente Vanillin oder eines deren Abbauprodukte einen Farbstoff bilden. In diesem Zusammenhang sei die sogenannte Orcinprobe erwähnt . Das dem Vanillin chemisch sehr nahe stehende Orcin reagiert mit einen aromatischen Aldehyd (Furfural) unter Bildung eines grünen Kondensationsproduktes:
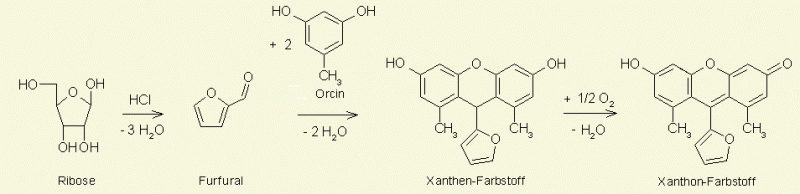
Siehe hierzu
http://www.chemieunterricht.de/dc2/kh/kh-farbreak.htm
http://www.demochem.de/p32_rib_rna.htm
Trotz intensiver Internetrecherche habe ich keinerlei Literatur zu meinem Experiment gefunden. Gefunden habe ich nur die sogenannte Günzburg-Reagenz (Gemisch aus Lösungen von Phlorogluzin u. Vanillin in Alkohol) zum Nachweis kleinster Mengen freier Salzsäure sowie eine Reagenz, die aus Vanillin und Schwefelsäure besteht, um Steroide nachzuweisen. Vielleicht kann der eine oder andere mein Experiment wiederholen und/oder hat andere Ideen, wie es zu der Grünfärbung kommt.
Viele Grüße,
Markus