H2O2 aufkonzentrieren
Moderator: Moderatoren
-
Plutonium242
- Illumina-Mitglied
- Beiträge: 56
- Registriert: Sonntag 18. April 2010, 16:30
- Wohnort: Freiburg im Breisgau
H2O2 aufkonzentrieren
Gibt es Methoden, um wasserstoffperoxid Lösung aufzukonzentrieren oder konzentrierte Lösungen herzustellen?
2H2O↔H3O+ + OH-
- frankie
- Illum.-Ass.
- Beiträge: 1941
- Registriert: Dienstag 10. April 2007, 17:00
- Wohnort: Res Publica Austria
UTFSE !
Aus einem alten Post von Karl-Heinz:

mfg
Gmelin Band 1, 1907Verdünnte Lösungen von Wasserstoffhyperoxyd konzentriert man am zweckmässigsten durch Ausfrierenlassen des Wassers. HOUZEAU. - Zur Darstellung von konz. H2O2 konzentriert man die gereinigte Lösung zuerst auf dem Wasserbade bis zu etwa 15 Vol.%; dann bringt man sie durch wiederholtes Gefrieren auf etwa 70 bis 80 Vol. Proz. und vollendet die Konzentration schließlich im trockenen Vakuum.
Aus einem alten Post von Karl-Heinz:


mfg
It is always better to have no ideas than false ones; to believe nothing, than to believe what is wrong.
(Thomas Jefferson)
(Thomas Jefferson)
-
Plutonium242
- Illumina-Mitglied
- Beiträge: 56
- Registriert: Sonntag 18. April 2010, 16:30
- Wohnort: Freiburg im Breisgau
- frankie
- Illum.-Ass.
- Beiträge: 1941
- Registriert: Dienstag 10. April 2007, 17:00
- Wohnort: Res Publica Austria
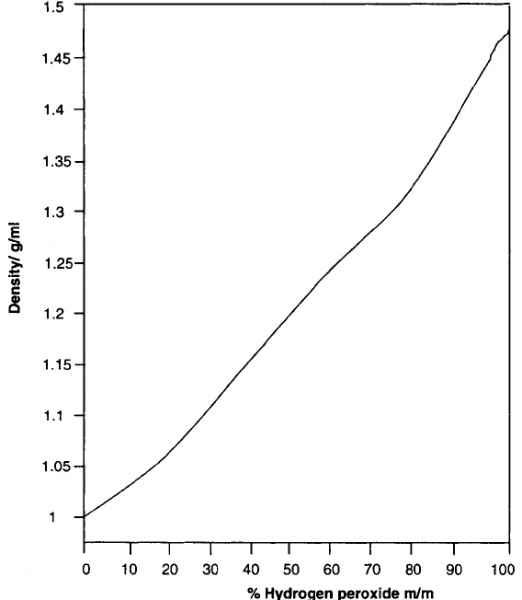
Lass das mit dem Destillieren; das ist hier sowieso keine allzu gute Idee. Versuche es mit Ausfrieren: Du musst aber sehr langsam abkühlen, und zwar dergestalt, dass sich keine Einschlüsse des Perhydrols im Wasser bilden und du schöne Eiskristalle erhältst. Abschließend kannst du vom Eis dekantieren. Mit Hilfe der Dichte-Tabelle kannst du herausfinden wie weit du gekommen bist (Falls du kein Pyknometer hast, kannst du auch einen kalibrierten Messkolben benutzen).
mfg
mfg
It is always better to have no ideas than false ones; to believe nothing, than to believe what is wrong.
(Thomas Jefferson)
(Thomas Jefferson)
-
Plutonium242
- Illumina-Mitglied
- Beiträge: 56
- Registriert: Sonntag 18. April 2010, 16:30
- Wohnort: Freiburg im Breisgau
Beim ersten Abkühlen kannst dus in ne Kühltruhe mit -18 machen, beim Zweiten mal würde ich dann nur noch -5 und beim dritten mal genau 0 grad. Kuck mal bei Wikipedia, da stehen die Werte
"Denkt ihr die Flüchtlinge sind in Partyboote gestiegen, mit dem großen Traum im Park mit Drogen zu dealen?"-K.I.Z.
-
Plutonium242
- Illumina-Mitglied
- Beiträge: 56
- Registriert: Sonntag 18. April 2010, 16:30
- Wohnort: Freiburg im Breisgau
-
Justus Liebig
- Illumina-Mitglied
- Beiträge: 298
- Registriert: Dienstag 25. Mai 2010, 13:04
- Wohnort: Bochum
-
Plutonium242
- Illumina-Mitglied
- Beiträge: 56
- Registriert: Sonntag 18. April 2010, 16:30
- Wohnort: Freiburg im Breisgau
- Timmopheus
- Illumina-Mitglied
- Beiträge: 919
- Registriert: Donnerstag 24. Juli 2008, 17:13
-
Justus Liebig
- Illumina-Mitglied
- Beiträge: 298
- Registriert: Dienstag 25. Mai 2010, 13:04
- Wohnort: Bochum
...mit entsprechender Kühlpower schon. Und vor allem würde ich den Versuch auf mehr als eine Nacht anlegen, besser mal ne Woche lang schön langsam runter mit der Temperatur.
Ich hätte es sonst noch mal mit einem Calciumchlorid-Eis-Bad versucht, aber der Kühleffekt wäre dann ja nur kurzfristig.
„Genie ist 1% Inspiration und 99% Transpiration.“
- dg7acg
- Illumina-Moderator
- Beiträge: 2665
- Registriert: Sonntag 15. Oktober 2006, 21:17
- Wohnort: Am Popo des Planeten
@Tim: ich schrieb ja auch "Normale Haushaltsgefriertruhen"!  Meine kann das z.B. nicht.
Meine kann das z.B. nicht.
Trockeneis hat den Nachteil, da nicht langsam mit runter zu kommen mit der Temperatur, da hats gleich volle Kälte.
Vor allem muss man es immer im Auge behalten und hin und wieder Eis nachlegen. Aber wer sich das antun will kanns auch damit mal versuchen...
Trockeneis hat den Nachteil, da nicht langsam mit runter zu kommen mit der Temperatur, da hats gleich volle Kälte.
Vor allem muss man es immer im Auge behalten und hin und wieder Eis nachlegen. Aber wer sich das antun will kanns auch damit mal versuchen...
...auf der Steuerflucht erschossen! 