Im Jahre 1828 synthetisierte Friedrich Wöhler Harnstoff aus Ammoniumcyanat. Zusammen mit seiner Synthese von Oxalsäure aus Dicyan widerlegte dies die Vitalismus-Theorie, die besagte, dass eine "Lebenskraft" (vis vitalis) für die Synthese organischer Stoffe aus anorganischen nötig sei. Deshalb stellt die Wöhlersche Harnstoffsynthese trotz ihrer einfachen Durchführung einen der wichtigsten Meilensteine der organischen Chemie dar. Wöhler schrieb über seine Entdeckung an Berzelius:
(Quelle: O. Wallach (Hg.). Briefwechsel zwischen J. Berzelius und F. Wöhler. Sändig Reprint Verlag, Vaduz, 1984.)Lieber Herr Professor!
Obgleich ich sicher hoffe, dass mein Brief vom 22. Jan. und das Postscript vom 2ten Februar bey Ihnen angelangt sind, und ich täglich oder vielmehr stündlich in der gespannten Hoffnung lebe, einen Brief von Ihnen zu erhalten, so will ich ihn doch nicht abwarten, sondern schon wieder schreiben, denn ich kann, so zu sagen, mein chemisches Wasser nicht halten und muss Ihnen sagen, dass ich Harnstoff machen kann, ohne dazu Nieren oder überhaupt ein Tier, sey es Mensch oder Hund, nöthig zu haben. Das cyansaure Ammoniak ist Harnstoff.
In diesem Versuch wird zunächst Kaliumcyanat durch Oxidation von Kaliumcyanid an der Luft hergestellt. Dann wird mit Ammoniumchlorid erhitzt, um über eine intermediäre Ammoniumcyanatlösung Harnstoff zu erhalten.
Geräte:
Porzellantiegel, Dreifuß, Tondreieck, Brenner, Spatel, Waage, Becherglas 50 ml, Trichter, Kristallisierschale
Chemikalien:
Kaliumcyanid


Wasser
Ammoniumchlorid
Aceton
Aktivkohle
Kaliumcyanat

Harnstoff
Kaliumchlorid
Hinweis:
Beim Erhitzen der Kaliumcyanat-Ammoniumchlorid-Lösung kann Cyanwasserstoff freigesetzt werden! Abzug!
Durchführung:
1,30 g Kaliumcyanid werden in einem Porzellantiegel vorsichtig erhitzt. Zunächst ist keine Veränderung zu beobachten, dann schmilzt das Pulver plötzlich recht schnell. Unter Rühren wird noch wenige Minuten weiter erhitzt und dann abkühlen gelassen. Die Masse wird nun in 15 ml Wasser gelöst und mit 1,07 g Ammoniumchlorid versetzt. Das Gemisch wird bis zur vollständigen Auflösung des Ammoniumchlorids gerührt und dann eingeengt, bis die Lösung eine sirupöse Konsistenz und bräunliche Farbe angenommen hat; das restliche Wasser lässt man bei Raumtemperatur verdampfen. Der Rückstand wird mit 20 ml Aceton und 0,1 g Aktivkohle zum Sieden erhitzt und abfiltriert. Falls der Extrakt nicht farblos ist wird weiter bis zur Farblosigkeit mit Aktivkohle behandelt. Nun wird der Extrakt in eine Kristallisierschale gegossen, um nach dem Verdampfen des Acetons Harnstoff in Form farbloser, langer Kristallnadeln zu hinterlassen.
Entsorgung:
Aceton wird zu den halogenfreien organischen Lösemittelabfällen gegeben. Aktivkohle wird zu den anorganischen Abfällen gegeben. Kaliumcyanid kann mit Eisen(II)-sulfat unschädlich gemacht werden. Alle anderen Stoffe können stark verdünnt in das Abwasser gegeben werden.
Erklärung:
Kaliumcyanid oxidiert beim Erhitzen an der Luft zu Kaliumcyanat:
2 KCN + O2 ---> 2 KOCN
Das macht sich durch das Schmelzen bemerkbar; Kaliumcyanat schmilzt bei 314°C während Kaliumcyanid erst bei 634°C schmelzen würde.
Bei Erwärmung kommt es zu einer Reaktion zwischen Ammonium- und Cyanationen. Dabei werden zunächst Cyansäure und Ammoniak gebildet:
NH4+ + O=C=N- ---> NH3 + O=C=NH
Der Ammoniak greift die Cyansäure nucleophil an und ein Proton wird vom einen auf das andere Stickstoffatom übertragen, wodurch sich Harnstoff bildet:
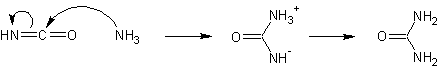
Bilder:

Oxidation von Kaliumcyanid

Erhitzen der Ammoniumchlorid-Kaliumcyanat-Lösung

Harnstoff


