Die Wittig-Reaktion ist eine sehr vielseitige Reaktion zur Synthese von (insbesondere asymmetrischen) Olefinen aus Carbonylverbindungen. Hier wird aus Benzyltriphenylphosphoniumchlorid und Zimtaldehyd 1,4-Diphenyl-1,3-butadien hergestellt, welches durch sein konjugiertes π-Elektronensystem ein hervorragender Fluorophor ist.
Geräte:
Erlenmeyerkolben 100 ml, Rührfisch, Magnetrührer, Apparatur zur Vakuumfiltration
Chemikalien:
Benzyltriphenylphosphoniumchlorid

Natriummethanolat
Methanol
N,N-Dimethylformamid
Zimtaldehyd
2-Propanol
1,4-Diphenyl-1,3-butadien
Durchführung:
5,00 g Benzyltriphenylphosphoniumchlorid werden in 30 ml N,N-Dimethylformamid suspendiert. Nun wird unter magnetischem Rühren langsam eine Lösung von 0,73 g Natriummethanolat in 10 ml Methanol zugegeben, wobei sich die farblose Suspension zinnoberrot färbt und der Feststoff vollständig gelöst wird. Tropfenweise werden 1,62 ml Zimtaldehyd zugegeben, wobei die Farbe nach gelb wechselt. Das Reaktionsgemisch wird noch 30 Minuten lang gerührt; dann werden 50 ml eines 2:1-Gemischs von Wasser und Methanol zugegeben. Der ausfallende gelbliche Feststoff wird abgesaugt, mit Wasser-Methanol-Gemisch nachgewaschen, mit 20 ml 2-Propanol verrührt und erneut abgesaugt. Ausbeute 0,83 g (31,3% d. Th.) 1,4-Diphenyl-1,3-butadien. Farblose, glänzende Kristalle, die unter UV-Licht hell blau fluoreszieren.
Entsorgung:
Benzyltriphenylphosphoniumchlorid und 1,4-Diphenyl-1,3-butadien werden zu den organischen Feststoffabfällen gegeben. Methanol, 2-Propanol, Zimtaldehyd und N,N-Dimethylformamid werden zu den halogenfreien organischen Lösemittelabfällen gegeben. Natriummethanolat kann in kleinen Mengen mit viel Wasser in den Abfluss gegeben werden.
Erklärung:
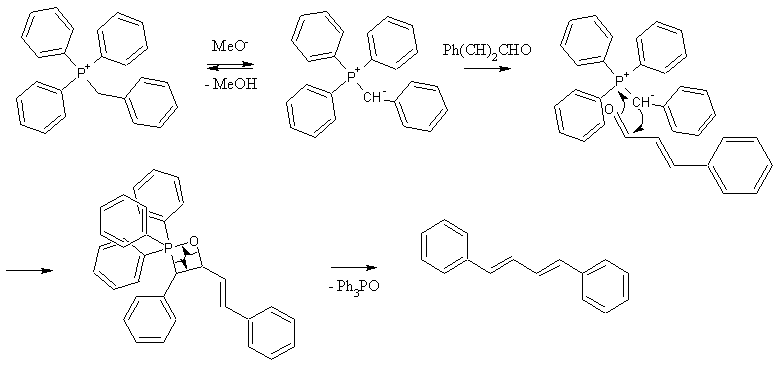
Das Benzyltriphenylphosphoniumchlorid wird vom Natriummethanolat unter Bildung eines Phosphorylids deprotoniert. Das Ylid kann dann mit einer Carbonylverbindung zu einem Oxaphosphetan reagieren, welches dann zum Olefin und Triphenylphosphinoxid zerfällt. Die Triebkraft für diese Reaktion liefert die Bildung der sehr stabilen P-O-Bindung.
Bilder:

Nach Zugabe des Natriummethanolats

Nach Zugabe des Zimtaldehyds

1,4-Diphenyl-1,3-butadien

Fluoreszenz des 1,4-Diphenyl-1,3-butadiens

Fluoreszenz von aus Cyclohexan rekristallisiertem 1,4-Diphenyl-1,3-butadien (Bild von NI2)

