Die Sandmeyer-Reaktion findet Anwendung in der Synthese von Arylhalogeniden, Phenolen und Nitrilen aus primären, aromatischen Aminen. Dabei treten geringe Mengen von Diarylen als Nebenprodukte auf, was auf einen radikalischen Reaktionsverlauf schließen lässt. Außerdem treten Azoverbindungen auf, da Diazoniumionen schwach elektrophil sind und sich so teilweise selbst/gegenseitig substituieren können.
Benannt nach: Traugott Sandmeyer (CH)
Entdeckung: 1884
Mechanismus:
Zunächst entsteht aus einem Amin und Nitrit in Mineralsäure ein Diazoniumion:
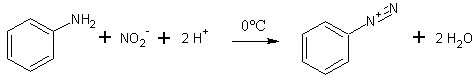
Dieses hat Stickstoff als gute Abgangsgruppe.
Durch den Zusatz eines Kupfer(I)-katalysators wird die eigentliche Reaktion gestartet: Das Diazoniumion oxidiert Cu+ zu Cu2+, spaltet dabei Stickstoff ab und wird zu einem Radikal:
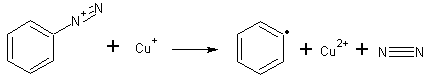
Dieses Radikal nimmt ein zugegebenes Nukleophil auf, wobei das Cu+ zurückgebildet wird:

Sandmeyer-Reaktion: Synthese von 4-Brom-2-nitrotoluol im Rahmen der Totalsynthese von Purpur
