Coffein
Moderator: Moderatoren
- Cyanwasserstoff
- Illumina-Admin
- Beiträge: 6303
- Registriert: Sonntag 7. Mai 2006, 20:41
- Kontaktdaten:
Ich war heute in Aachen und habe das 1H-NMR-Spektrum anfertigen lassen. Ich habe etwa 5 mg doppelt sublimiertes Coffein in 0,5 ml Deuterochloroform gelöst und in ein NMR-Vial überführt. Dann bin ich mit einer Assistentin in den Messraum mit 6 NMR-Spektrometern gegangen, wo dann mit einem 300 MHz NMR-Spektrometer von Bruker gemessen wurde. Hier das Spektrum:

Sieht soweit also schonmal ganz gut aus. Nun versuche ich mich mal an der Auswertung.
Zur Veranschaulichung nochmal die Strukturformel des Coffeins mit allen Wasserstoffatomen:
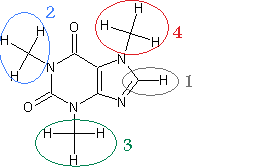
Der Peak bei 7,44 ppm ist auf das in der Strukturformel mit 1 gekennzeichnete Proton zurückzuführen. Durch den starken -I-Effekt der beiden Stickstoffatome kommt es zu starkem Deshielding und somit zu einem großen Shift. Der Peak bei 7,20 ppm beruht auf den Restprotonen des Lösemittels (das CDCl3 hatte einen Deuterierungsgrad von 99,8%). Der Peak bei 3,93 ppm ist auf die Protonen der mit 2 gekennzeichneten Methylgruppe zurückzuführen, durch den Stickstoff mit zwei angrenzenden Carbonylgruppen kommt es auch hier zu stärkerem Shift als bei Methylgruppe 3 (3,52 ppm), bei der an den Stickstoff nur eine Carbonylgruppe angrenzt und als bei Methylgruppe 4 (3,35 ppm), bei der gar keine Carbonylgruppen angrenzen. Das Verhältnis der Integrale dieser Peaks stimmt mit dem anhand der Strukturformel zu erwartenden Verhältnis überein; wie zu erwarten war tritt kein Splitting auf, d.h. alle Peaks sind Singlets. Es bleibt noch ein Peak bei 1,54 ppm, den ich nicht zuordnen kann.

Sieht soweit also schonmal ganz gut aus. Nun versuche ich mich mal an der Auswertung.
Zur Veranschaulichung nochmal die Strukturformel des Coffeins mit allen Wasserstoffatomen:

Der Peak bei 7,44 ppm ist auf das in der Strukturformel mit 1 gekennzeichnete Proton zurückzuführen. Durch den starken -I-Effekt der beiden Stickstoffatome kommt es zu starkem Deshielding und somit zu einem großen Shift. Der Peak bei 7,20 ppm beruht auf den Restprotonen des Lösemittels (das CDCl3 hatte einen Deuterierungsgrad von 99,8%). Der Peak bei 3,93 ppm ist auf die Protonen der mit 2 gekennzeichneten Methylgruppe zurückzuführen, durch den Stickstoff mit zwei angrenzenden Carbonylgruppen kommt es auch hier zu stärkerem Shift als bei Methylgruppe 3 (3,52 ppm), bei der an den Stickstoff nur eine Carbonylgruppe angrenzt und als bei Methylgruppe 4 (3,35 ppm), bei der gar keine Carbonylgruppen angrenzen. Das Verhältnis der Integrale dieser Peaks stimmt mit dem anhand der Strukturformel zu erwartenden Verhältnis überein; wie zu erwarten war tritt kein Splitting auf, d.h. alle Peaks sind Singlets. Es bleibt noch ein Peak bei 1,54 ppm, den ich nicht zuordnen kann.
"It is arguably true that the tetrapyrrole system is Nature's most remarkable creation."
- Claude Rimington
- Claude Rimington
- Cyanwasserstoff
- Illumina-Admin
- Beiträge: 6303
- Registriert: Sonntag 7. Mai 2006, 20:41
- Kontaktdaten:
Ein Massenspektrum habe ich nun auch eingefügt. Damit niemand ernsthaft auch nur auf die Idee kommen könnte, das Coffein wäre nicht ausreichend analysiert worden, habe ich aus dem ganzen ein LC-(TIC)-MS gemacht bzw. machen lassen und außerdem auch noch ein IR-Spektrum aufnehmen lassen. Die werde ich jetzt aber nicht auch noch interpretieren, das überlasse ich vorerst dem geneigten Leser.
"It is arguably true that the tetrapyrrole system is Nature's most remarkable creation."
- Claude Rimington
- Claude Rimington
- Kohlenstoff
- Illumina-Mitglied
- Beiträge: 1250
- Registriert: Dienstag 26. Februar 2008, 19:59
- Wohnort: Kreis Aachen
- Cyanwasserstoff
- Illumina-Admin
- Beiträge: 6303
- Registriert: Sonntag 7. Mai 2006, 20:41
- Kontaktdaten:
Naja, die genaue Reinheit kann man an den Spektren auch nicht ablesen. Im NMR-Spektrum ist halt ein Peak, der nicht da hingehört, die Peaks im IR-Spektrum muss ich mir alle nochmal genauer ansehen um zu sehen ob auch wirklich nur die zu erwartenden funktionellen Gruppen dabei sind oder was sonst noch da ist. Am hilfreichsten dürfte der Graph der LC sein, der schon eine ganz gute Reinheit vermuten lässt.
"It is arguably true that the tetrapyrrole system is Nature's most remarkable creation."
- Claude Rimington
- Claude Rimington
-
Bariumchlorid
- Illumina-Mitglied
- Beiträge: 1570
- Registriert: Samstag 6. Juni 2009, 21:37
Abend 
Also ich habe mir das Massenspektrum grade mal angesehen und soweit ist auch alles klar, der Peak bei 194,2 is der Molekülionenpeak und der entspricht auch der Mol-Masse des Coffeins. Jedoch kommen danach noch weitere Peaks, auch rechts vom MIP, was ich recht komisch finde. Sind das Isotopenpeaks oder ist das ne höhermolekulare Verunreinigung ?
Also ich habe mir das Massenspektrum grade mal angesehen und soweit ist auch alles klar, der Peak bei 194,2 is der Molekülionenpeak und der entspricht auch der Mol-Masse des Coffeins. Jedoch kommen danach noch weitere Peaks, auch rechts vom MIP, was ich recht komisch finde. Sind das Isotopenpeaks oder ist das ne höhermolekulare Verunreinigung ?
- Cyanwasserstoff
- Illumina-Admin
- Beiträge: 6303
- Registriert: Sonntag 7. Mai 2006, 20:41
- Kontaktdaten:
- Uranhexafluorid
- Illumina-Mitglied
- Beiträge: 145
- Registriert: Donnerstag 10. September 2009, 21:41
-
Bariumchlorid
- Illumina-Mitglied
- Beiträge: 1570
- Registriert: Samstag 6. Juni 2009, 21:37
Wuerde rechnerisch hinhaun, wollte mich nur vergewissern...
Ich sprach mit Felix noch generell darüber und er meinte, dass auch aus dem entstandenen Ionen wieder neue Ionen entstehen können, was ich für durchaus plausibel halte. Das würde dann auch den höheren Peak erklären, wobei eine Protonierung, welche Jan ansprach für mich nur schlecht erklärlich ist, denn die x-Achse kennzeichnet das Verhältnis m/z.
Ich sprach mit Felix noch generell darüber und er meinte, dass auch aus dem entstandenen Ionen wieder neue Ionen entstehen können, was ich für durchaus plausibel halte. Das würde dann auch den höheren Peak erklären, wobei eine Protonierung, welche Jan ansprach für mich nur schlecht erklärlich ist, denn die x-Achse kennzeichnet das Verhältnis m/z.
-
6,6´-Dibromindigo
- Illumina-Mitglied
- Beiträge: 66
- Registriert: Freitag 19. August 2011, 20:54
Ich habe herrausgefunden, dass die Reduktion zum Diaminouracil sich außer mit Sulfid oder H2 anscheinend auch mit Dithionit bewerkstelligen lässt. Im Gattermann-Wieland ist dazu eine Vorschrift, die eine 50-55%-ige Ausbeute dafür angiebt. Außerdem ist dieser Weg hier beschrieben: http://www.orgsyn.org/orgsyn/orgsyn/pre ... p=cv4p0247 (Nebenbei interessant die Zusammenfassung der ersten beiden Stufen in dieser Vorschrift).
Ich werde das mal ausprobieren.
Ich werde das mal ausprobieren.
-
Algi0506
- Illumina-Mitglied
- Beiträge: 36
- Registriert: Montag 5. Januar 2015, 08:15
- Wohnort: Niederösterreich
Coffein Extraktion
Dadurch dass ich diese Ausgangsstoffe nicht zur Verfügung habe, möchte ich hier fragen, ob jemand so nett sein könnte und mir schreiben könnte, wie man das Coffein aus Kaffeebohnen extrahiert?
Rein theortisch könnte man Kaffeesud in H2O erhitzen, zum Lösen (in H2O löst sich Coffein besser als in Ethanol). Dann das Wasser verdampfen und die Reste bei ca 180°C sublimieren, dass an einer kalten Oberfläche kondensierte und erstarrrte Coffein müsste dann auch ziemlich rein sein oder?
Wahrscheinlich ist das für euch ganz logisch, aber ich kenn mich in der Chemie noch nicht so gut aus.
Mfg
Rein theortisch könnte man Kaffeesud in H2O erhitzen, zum Lösen (in H2O löst sich Coffein besser als in Ethanol). Dann das Wasser verdampfen und die Reste bei ca 180°C sublimieren, dass an einer kalten Oberfläche kondensierte und erstarrrte Coffein müsste dann auch ziemlich rein sein oder?
Wahrscheinlich ist das für euch ganz logisch, aber ich kenn mich in der Chemie noch nicht so gut aus.
Mfg
Dazu gibt's genug im Netz, aber ein Tipp: vorher das Kaffee pulver trocknen!! Andernfalls wird die Sublimation schlonzig, weil Wasser mit kondensiert. (Hatte es selbst mal quick'n'dirty probiert aber da er nicht getrocknet war hab ich's nicht weiter verfolgt.)
I❤OC
There is no sadder sight in the world than to see a beautiful theory killed by a brutal fact. [T. Huxley]
The pursuit of knowledge is hopeless and eternal. Hooray! [Prof. H. J. Farnsworth]
Trust the rhythm and the rhyme of your own heartbeat. [C. Douglas]
There is no sadder sight in the world than to see a beautiful theory killed by a brutal fact. [T. Huxley]
The pursuit of knowledge is hopeless and eternal. Hooray! [Prof. H. J. Farnsworth]
Trust the rhythm and the rhyme of your own heartbeat. [C. Douglas]
Molare Umsetzung?
Hi,
Sind deine Angaben für die Synthese auf deine Ausbeute bezogen?
LG ChemTim
Sind deine Angaben für die Synthese auf deine Ausbeute bezogen?
LG ChemTim