--> Überraschungsgast
Beim - manchmal eher trockenen - Durchgehen möglicher Mischungsbestandteile gibt es jetzt mal eine Überraschung, die bisher keiner von uns erwähnt hat. Interessanterweise ist diese einfache Verbindung sogar im ganzen Forum noch nicht vorgekommen. Aber erstmal der Reihe nach:
Essigsäure konnte als Hauptursache für das stärkste Maximum bei 206 nm hier
https://illumina-chemie.org/spiritus--gl ... html#72132 ff. ausgeschlossen werden. Genauso Ethylacetat, welches ebenfalls höchstens untergeordnet zum Maximum beiträgt
https://illumina-chemie.org/spiritus--gl ... html#72055 . Aufgrund der ähnlichen Absorptionscharakteristik und Flüchtigkeit sind damit auch die höheren aliphatischen Carbonsäuren und Ester sowie Ameisensäure
http://satellite.mpic.de/spectral_atlas ... C(O)OH.spc und die Ameisensäureester
http://satellite.mpic.de/spectral_atlas ... )OC2H5.spc ausgeschlossen.
Damit bleibt die Frage, was es denn sonst noch sein könnte. Um 206 nm hat das "Organische Chemie" von Allinger Carbonsäuren, Alkine, konjugierte Diene, Sulfoxide, Benzol und den pi-pi*-Übergang von Carbonylverbindungen. Das "Practical HPLC Method Development" von Snyder hat in dem Bereich CHO, COOH, COOR, C=C-C=C, C=C=C=O soll wahrscheinlich C=C-C=O sein, C=C-C=N, Salpetrigsäureester, Nitrogruppen, Sulfoxide, Thioether, Thioketone sowie Benzol. Die schwefelhaltigen Stoffgruppen würde ich weglassen, da sollte nichts enthalten sein. An Stickstoff würden mit der Info von
https://de.wikipedia.org/wiki/Verg%C3%A4llungsmittel
Seit dem 1. Juli 2013 ist zur vollständigen Vergällung von Ethanol EU-einheitlich der Zusatz folgenden Gemisches auf 100 Liter absoluten Ethanols vorgeschrieben:[2]
3 Liter Isopropylalkohol (Propan-2-ol) (IPA),
3 Liter Methylethylketon (Butan-2-on) (MEK) und
1 Gramm Denatoniumbenzoat
... In Deutschland muss dem Alkohol aufgrund dieser Rechtsänderung ab dem 1. August 2017 je 100 Liter Alkohol
1 Liter Isopropylalkohol (Propan-2-ol) (IPA),
1 Liter Methylethylketon (Butan-2-on) (MEK) und
1 Gramm Denatoniumbenzoat (Bitrex)
zugefügt werden ...
aus dem Denatoniumbenzoat mit einem Massenanteil von Stickstoff von 2*14/446,58=6,3% auch nur 0,63 mg/l bzw. 45 µmol/l N im Spiritus enthalten sein. Bei so niedrigen Konzentrationen würden nur starke Absorptionen sichtbar sein, was für die Salpetrigsäureester, Nitroverbindungen und C=C-C=N zutreffen würde. Aus Bitrex könnten bei der Pyrolyse auch andere Aromaten entstehen.
Es bleiben also diese Kandidaten:
Alkine
konjugierte Diene
Aromaten
Carbonylverbindungen
C=C-C=N
Salpetrigsäureester
Nitrogruppen
Salpetrigsäureester absorbieren wie Methylnitrit
http://satellite.mpic.de/spectral_atlas ... CH3ONO.spc eher über 215 nm und haben weitere Banden um 350 nm. Passen also nicht.
Nitroalkane wie Nitromethan absorbieren stark im richtigen Bereich, aber die verfügbaren Gasphasenspektren weichen untereinander zu stark ab um als Bestätigung verwendet werden zu können:
http://satellite.mpic.de/spectral_atlas ... CH3NO2.spc . Die Entstehung aus Denatoniumbenzoat (quartäres Ammoniumsalz und Amid) kann ich mir aber ohne Sauerstoffzufuhr eher schwer vorstellen.
Acetylen als hier noch am ehesten zu erwartendes Alkin absorbiert nach
http://satellite.mpic.de/spectral_atlas ... s/C2H2.spc in Form einer sehr breiten Bande, die von 220 bis 190 nm immer nur weiter ansteigt ohne ausgeprägtes dazwischenliegendes Maximum. Passt von der Form her also nicht für das Maximum, könnte aber trotzdem auch enthalten sein.
Bei Benzol und substituierten Benzolen wären zusätzlich mehrere Banden im Bereich um 250 nm zu erwarten, die fehlen:
http://satellite.mpic.de/spectral_atlas ... l/C6H6.spc .
Das einfachste konjugierte Dien 1,3-Butadien würde in dem Bereich absorbieren, allerdings mit einer starken Feinstruktur, während meine Bande ziemlich glatt ist. Das hätte ich selbst mit meiner Bandbreite von 6 nm sehen müssen:
http://satellite.mpic.de/spectral_atlas ... CH=CH2.spc . Die Derivate mit mehr Alkylketten absorbieren bei noch höheren - zu hohen - Wellenlängen.
Acetaldehyd selbst hat seinen pi->pi*-Übergang bei niedrigeren Wellenlängen unter 200 nm und kommt damit auch nicht in Frage:
https://illumina-chemie.org/spiritus--gl ... html#72221 . Ähnlich sieht es für die höheren aliphatischen Aldehyde aus. Formaldehyd absorbiert ganz anders mit mehreren Banden von 300 bis 340 nm, die es bei mir nicht gibt, und ist damit auch raus:
http://satellite.mpic.de/spectral_atlas ... )/CH2O.spc
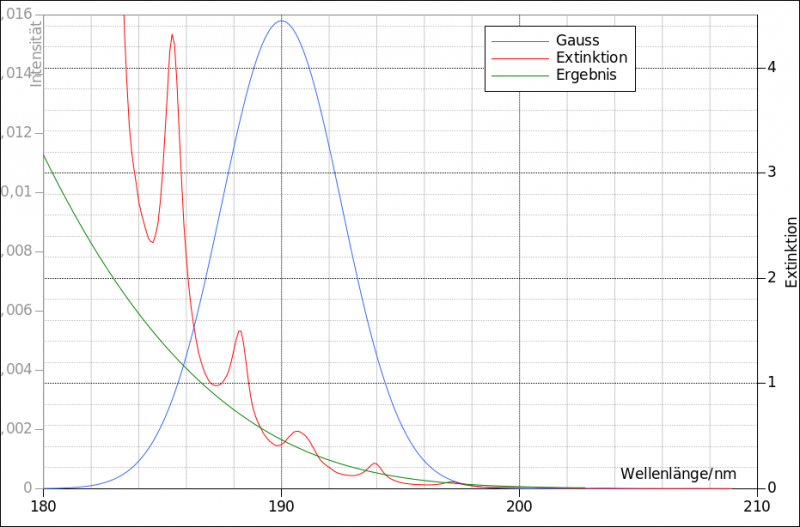
Wesentlich besser passen die α,β-ungesättigten Carbonylverbindungen mit einem Maximum des pi->pi*-Übergang um 200 nm. Von denen liegt mit 204 nm der Crotonaldehyd / trans-2-Butenal besonders nah an meinen 206 nm:

Quelle Referenzspektrum (rot): Keller-Rudek, H. et al. - CH3CH=CHCHO_VUV_lin.jpg von
http://satellite.mpic.de/spectral_atlas ... =CHCHO.spc
Die Bildung von Crotonaldehyd aus Ethanol ist dabei über Acetaldehyd und dessen Aldolkondensation plausibel. Mit einem Siedepunkt von 102 °C ist er auch ausreichend flüchtig um in der Gasphase aufzutauchen.
Nehmen wir mal an, dass der Crotonaldehyd den Hauptteil der Absorption bei 206 nm ausmacht: Sein Absorptionsquerschnitt beim Maximum bei 204 nm liegt bei 6e-17 cm². Das entspräche einer Extinktion von etwa 6e-17 cm² * 2,615e20 mol⁻¹ * 0,04 mol l⁻¹ * 1 cm = 628 für blanken, idealen, massiv übersättigten Crotonaldehyddampf bei 25 °C und 1 bar. (Einzelheiten zur Berechnung siehe
https://illumina-chemie.org/spiritus--gl ... html#72038). Die maximale Absorption in den gemessenen Spektren liegt mit 0,76 weit darunter. D.h. die Bande bei 206 nm könnte leicht allein durch Crotonaldehyd erklärt werden, bis auf die 2 nm Differenz. Der Gehalt wäre dann 0,76 / 628 = 1,2e-3 also 0,12 Mol-%, was gleichzeitig die Obergrenze für den möglichen Gehalt an Crotonaldehyd wäre.
Dass höchstens wenig Crotonaldehyd enthalten ist, ist hier vorläufig eher von Vorteil, bei einem schweizer MAK-Wert von 0,34 ml·m⁻³
https://www.bag.admin.ch/dam/bag/en/dok ... z-2016.pdf . Wobei es die Schweizer im Gegensatz zu
http://gestis.itrust.de/nxt/gateway.dll ... lt.htm$3.0 gerade nicht als mutagen oder krebserregend eingestuft haben. Den MAK-Wert könnte ich mit 0,34 ml/m³ / 1,2e-3 = 0,28 l/m³ oder 0,028 Vol.-% meiner Gasmischung erreichen. Anders ausgedrückt: Die bis zu 1 ml/s Mischung entsprechen bis zu 1,2e-3 ml/s oder 0,072 ml/min Crotonaldehyddampf. Um den MAK-Wert einzuhalten müsste die Mischung also mit 0,072 ml/min | 0,34 ml/m³ = 0,21 m³/min verdünnt werden. Ist bei etwas Wind und Abstand kein Problem, das Verbrennen des überschüssigen Gases ist aber noch besser. Der Hauptteil des Crotonaldehyds sollte allerdings im flüssigen Rückstand der Pyrolyse enthalten sein.
Crotonaldehyd hätte noch eine weitere Bande bei 330 nm, allerdings mit einer Intensität von nur etwa 0,1% der Bande bei 204 nm. D.h. bei meiner Mischung wäre eine Extinktion von bis zu 0,76*0,1% = 0,00076 zu erwarten. Die wäre nicht mehr messbar und da ist auch im Spektrum nichts zu sehen.
Crotonaldehyd könnte mit Aminen aus dem Denatonium dann theoretisch auch zu α,β-ungesättigten Schiffschen Basen mit Grundgerüst C=C-C=N reagieren. Allerdings wäre das dann eine Reaktion zwischen zwei nur in niedriger Konzentration enthaltenen Bestandteilen.
--> Wahrscheinlich leisten bis zu 0,12 % trans-2-Butenal den Hauptbeitrag für die stärkste Bande bei 206 nm