(Diphenylanthracen, DPA)
Diphenylanthracen ist ein Chemiluminiszenzfarbstoff, welcher sowohl als Feststoff, als auch in Lösung blau fluoresziert. Eine alternative Darstellung kann unter Einbuße der Ausbeute in einer zweistufigen Synthese aus Phenylmagnesiumbromid (oder Phenyllithium) und Anthrachinon erfolgen. Bei der hier beschriebenen Methode handelt es sich um eine palladiumkatalysierte Kreuzkupplung.
Geräte:
Magnetheizrührer inkl. Rührfisch, Ölbad, Mehrhals-Rundkolben, Rückflusskühler, Septum, Argon, Destillationsapparatur, Vakuumfiltrationsapparatur
Chemikalien:
9,10-Dibromanthracen


Benzolboronsäure
Tetrakis(triphenylphosphin)palladium(0)
Natriumcarbonat
Toluol
Kieselgel 60
2-Propanol
Petrolether
9,10-Diphenylanthracen
Durchführung:
In einem Rundkolben mit Septum werden 960 mg 9,10-Dibromanthracen und 1,1 g Benzolboronsäure in 3,9 mL einer 2 mol/L Natriumcarbonat-Lösung und 30 mL Toluol suspendiert. Anschließend wird die Luft aus der Apparatur mit Argon verdrängt und mit 110 mg Tetrakis(triphenylphosphin)palladium(0) versetzt. Unter leichtem Argonstrom wird die Reaktionsmischung 10 h unter Rückfluss gekocht. Nach beendeter Reaktion wird das Toluol abrotiert, zum Entfernen von Wasserresten mit wenigen Millilitern 2-Propanol versetzt und nochmals bis zur Trockne einrotiert. Der Rückstand wird in Toluol suspendiert, über ein Kieselgelpad filtriert und solange mit Toluol gewaschen, bis das weitere Filtrat nicht mehr fluoresziert.
Die vereinigten Filtrate werden auf einige Milliliter eingeengt, so dass nach dem Abkühlen das Diphenylanthracen auskristallisiert. Die erhaltenen Kristalle werden ggf. aus Toluol umkristallisiert, mit Petrolether gewaschen und im Vakuum getrocknet.
Ausbeute konnte nicht bestimmt werden.
Entsorgung:
Die verwendeten Lösungsmittel werden aufgearbeitet oder in die halogenfreien organischen Lösungsmittel gegeben. Das Dibromanthracen wird zu den halogenhaltigen organischen Abfällen gegeben, das Produkt wird aufbewahrt oder in die halogenfreien organischen Abfälle gegeben.
Erklärung:
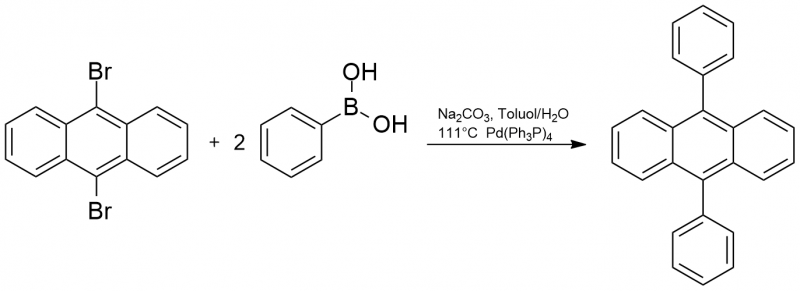
In einer Suzuki-Kupplung reagiert die Benzolboronsäure mit dem 9,10-Dibromanthracen, unter Bildung von 9,10-Diphenylanthracen.
Bilder:

Reaktionsapparatur

Fluoreszenz des siedenden Reaktionsgemisches
Vielen Dank an NI2 für sein Engagement und die Bereitstellung einiger der benötigten Reagenzien.