Geräte:
100ml-Rundkolben, Bechergläser, Magnetrührer, Vakuumfiltrationsequipment
Chemikalien:
Anthracen-9-carbaldehyd

Benzyltriphenylphosphoniumchlorid

Natronlauge 50%

Isopropanol


N,N-Dimethylformamid

trans-9-(2-phenylethenyl)-anthracen
Hinweis:
Bei der Synthese sollte unter dem Abzug gearbeitet werden. Besonders beim Umgang mit Dimethylfromamid sollten Handschuhe getragen werden.
Durchführung:
In einem 100 ml-Rundkolben werden 1,15 g Anthracen-9-carbaldehyd und 2 g Benzyltriphenylphosphoniumchlorid vorgelegt. Es werden 5 ml Dimethylformamid hinzugegeben und unter kräftigen Rühren eine Suspension erzeugt. In diese tropft man innerhalb von 10 Minuten insgesamt 3 ml 50% Natronlauge. Wärend der Zugabe der Natronlauge kann man eine Verfärbung der Suspension von gelb zu gelb-schwarz und eine Erwärmung des Gemisches feststellen. Nachdem die Natronlauge zugegeben wurde, wird noch 2 Stunden weiter gerührt, wobei sich das das Reaktionsgemisch nach dunkel-braun verfärbt. Jetzt gibt man ein Gemisch von 20 ml 2-Propanol und 20 ml Wasser hinzu, wobei sofort ein hellgelbes Produkt ausfällt, welches man mittels eines Büchnertrichters durch Vakuumfiltration abtrennt. Der Filterkuchen wird mit wenig 2-Propanol/Wasser (50:50) gewaschen.
Ausbeute: 1,08 g (70 % d.Th.)
Entsorgung:
Benzyltriphenylphosphoniumchlorid kommt in den organischen halogenhaltigen Abfall. Alle anderen Abfälle kommen in den organischen halogenfreien Abfall.
Erklärung:
Bei dieser Synthese findet eine Wittig-Reaktion statt. Eine Deprotonierung des Benzyltriphenylphosphoniumchlorids liefert ein Phosphorylid, welches mit Anthracen-9-carbaldehyd zu einem 1,2-Oxaphosphetan reagiert. Dessen Cycloreversion führt zur Bildung eines Alkens, wobei die Triebkraft der Reaktion aus der gleichzeitigen Bildung sehr stabilen Triphenylphosphinoxids stammt.
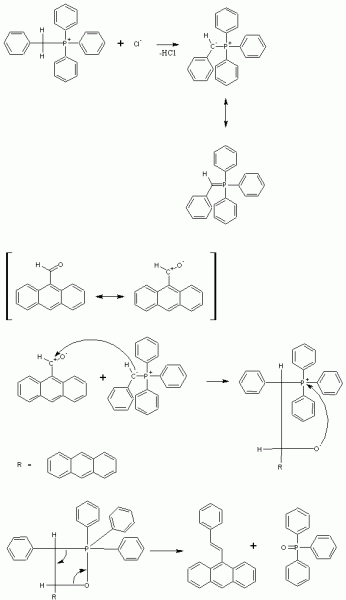
Bilder:

Vor der Reaktion

Während Zugabe der Natronlauge

Nach zwei Stunden Rühren

Einzelne Kristalle des Produkts (Bild von NI2)

Kristalle unter UV (366 nm) (Bild von NI2)

Fluoreszenz einer Lösung in DCM (Bild von NI2)

Die Chemolumineszenz
