Dieser Artikel beschreibt eine zweistufige Synthese, einerseits eine einfache N-Acetylierung, andererseits eine Erlenmeyersynthese, benannt nach ihrem Erfinder Emil Erlenmeyer, einer Abwandlung der Perkin-Synthese. Ihr Ziel ist es, durch Kondensation und Ringschluss einen Heterocyclus, ein Oxazim zu erhalten und dieses anschließend zum Azlacton der Acetylaminozimtsäure umzuwandeln.
Geräte:
Becherglas 250 ml, Magnetheizrührer, Destille, Rückflusskühler, Stativ, Trockenschrank, Exsikkator
Chemikalien:
Glycin
Essigsäureanhydrid
Benzaldehyd
Natriumacetat
Diethylether
Wasser
Durchführung:
6,25 g 2-Aminoessigsäure (Glycin) werden in 25 ml Wasser unter Rühren und Erwärmen gelöst. Danach werden 18 g Essigsäureanhydrid in einer Portion hinzugefügt und 25 Minuten gerührt, wobei sich das Reaktionsgemisch erwärmt und auszukristallisieren beginnt. Der Reaktionsansatz wird über Nacht in den Kühlschrank gestellt; am darauffolgenden Tag wird das Produkt abgesaugt, mit kaltem Wasser mehrmals gewaschen und anschließend eine Stunde bei 100°C im Trockenschrank getrocknet. (Ausbeute: 6,1g | 62% d.Th)
6,10 g des getrockneten und gereinigten Acetylglycins (Schritt I), 3,1 g wasserfreies Natriumacetat, 7,8 ml im Vakuum oder unter Inertgasatmosphäre frisch destillierter (!) Benzaldehyd sowie 13 ml Essigsäureanhydrid werden bei etwa 70°C gelöst und für etwa 1,5 Stunden im siedenden Wasserbad unter Rückfluss erhitzt. Die erhaltene, noch heiße gelb-braune Masse wird in ein geeignetes Gefäß überführt und zur Kristallisation über Nacht in den Kühlschrank gestellt. Das Produkt wird mit einer Nutsche abgesaugt und mit kaltem Wasser gewaschen.
Hinweis:: Es muss auf jeden Fall möglichst feinporiges Filterpapier resp. eine äquivalente Fritte verwendet werden. Der Ausbeuteverlust ist leider groß.
Um Reste des Benzaldehyds zu entfernen, wird das erhaltene Rohprodukt in einer Reibschale mit wenig kaltem Wasser zerrieben und erneut abgesaugt. Diese Prozedur wird 3 mal wiederholt. Anschließend wird das Produkt mit 15 ml eiskaltem Diethylether gewaschen, bis kein Benzaldehyd mehr vorhanden ist. Das Produkt wird bis zur Massenkonstanz im Exsikkator über Silicagel (besser Phosphorpentoxid) mehrere Tage lang getrocknet. Schmelzpunkt: XXX°C (Literatur: 148°C). [folgt nächstes Jahr]
Ausbeute: XX,XX g (XX,X% d.Th.) [folgt nächstes Jahr]
Entsorgung
Reste des Acetylglycins sowie des 2-Methyl-4-(phenylmethylen)-4H-oxazol-5-on kommen zu den organischen Abfällen.
Erklärung:
Es erfolgt durch Acetanhydrid eine N-Acetylierung am Glycin.
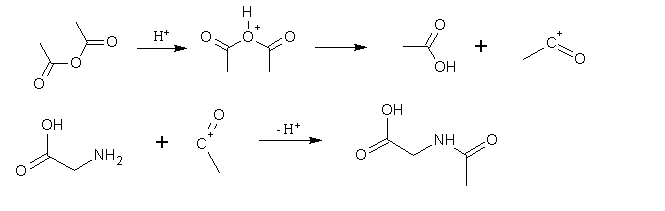
Nach Protonierung des Carbonylsauerstoffs und des dadurch entstandenen positivierten Kohlenstoffs wandert ein freies Elektronenpaar des Carboxylsauerstoffs zu dieser Position und es kommt zu einem Ringschluss. Das Proton des Oxoniumions wird abgespalten. Die Hydroxylgruppe entreißt dem Stickstoffatom sein verbleibendes Wasserstoffatom und spaltet dabei Wasser ab; die Irreversibilität dieser Abspaltung wird durch die Irreversibilität der Reaktion zwischen Acetanhydrid und dem entstehenden Wasser bedingt. Es entsteht eine Doppelbindung.
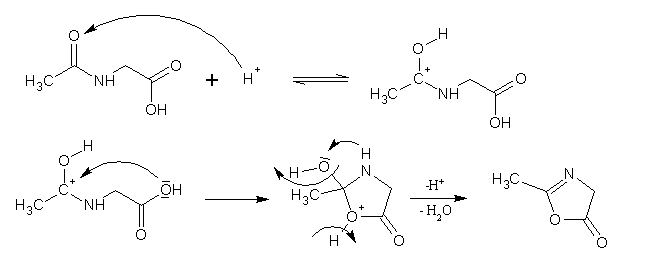
Zwischen Benzaldehyd und dem CH-aciden Azlacton kommt es zu einer Aldolreaktion.
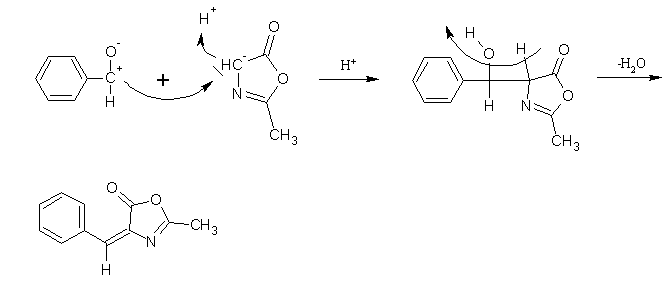
Bilder:

Synthese von Acetylglycin

Acetylglycin

Zu Beginn der Erlenmeyer-Reaktion

15 Minuten später (70°C) ...

Eine halbe Stunde später ... (~95°C)

Nach etwa 1 Stunde ...

Entfernung des Benzaldehyds

Getrocknetes Produkt

