Im Labor wird Wasserstoff üblicherweise durch Einwirkung von Säuren auf Metalle dargestellt. In diesem Experiment wird Wasserstoff aus Wasser und Magnesium-Pulver dargestellt.
Geräte:
Erlenmeyerkolben oder Rundkolben 200-300 mL, Gummistopfen mit Gasableitungsrohr und Schlauch, Stativ mit Muffe und Stativklennme für einen Kolben, Dreifuß mit Drahtnetz, Bunsen- oder Kartuschenbrenner, pneumatische Wanne mit Wasser, mit Wasser gefüllte Reagenzgläser zum Auffangen des Gases mit Stopfen, Reagenzglashalter, Waage und ggf. Messzylinder, Spatel
Chemikalien:
Magnesium-Pulver

Magnesiumchlorid Hexahydrat

Wasserstoff
Hinweis:
Magnesium-Pulver ist leicht entzündlich; der entstehende Wasserstoff ist hochentzündlich und kann explosiv sein. Es ist größte Vorsicht geboten mit offenen Zündquellen und Flammen! Magnesiumchlorid ist gemäß GHS als "reizend" eingestuft.
Durchführung:
2 g Magnesium-Pulver werden in einen Kolben vorgelegt und mit 50 mL Wasser übergossen. Um die Gasentwicklung zu beschleunigen, setzt man dem Wasser zweckmäßigerweise etwas Magnesiumchlorid zu; dieses beteiligt sich nicht weiter an der Reaktion, bringt aber entstehendes Magnesiumoxid zur Lösung und befreit das Metallpulver von einem Überzug, welcher die Einwirkung von Wasser erschweren würde. Der Kolben wird mit einem durchbohrten Gummistopfen verschlossen, in dem ein Gasbleitungsrohr mit Schlauch steckt. Nun wird der Kolben am Stativ befestigt auf den Dreifuß gestellt. Der Schlauch soll in das Wasser der pneumatischen Wanne reichen.
Der Kolben wird mit kleiner Flamme erwärmt. Die ersten Gasblasen verwirft man (viel Luft durch das Volumen des Kolbens). Setzt eine gleichmäßige Gasentwicklung ein, wird das Gas in mit Wasser gefüllten Reagenzgläsern aufgefangen und diese mit Stopfen verschlossen. Da Wasserstoff leichter als Luft ist, ist die Mündung bzw. Öffnung des Reagenzglases nach unten zu halten und dann zu öffnen. Anderenfalls verflüchtigt sich der Wasserstoff sofort und vermischt sich mit der Raumluft.
Ein Reagenzglas mit dem Gas wird mit der Mündung nach unten zu einer Flamme geführt und das Gas so angezündet. Zur Sicherheit hält man das Glas mit einem Reagenzglashalter der Flamme entgegen und trägt eine Schutzbrille. Das Gas wird mit einem leisen Geräusch und bläulicher - kaum sichtbarer - Flamme verbrennen. An den kühleren Stellen des Glases schlägt sich das Verbrennungsprodukt - Wasser - nieder. Ein stärkeres pfeifendes Geräusch oder gar Knall weisen darauf hin, dass der Wasserstoff noch nicht frei von Luft ist. Erst wenn der Wasserstoff ruhig brennt - also die "Knallgasprobe" negativ erläuft -, sollten erst größere Gefäße damit gefüllt werden.
Bevor der Brenner wegen nachlassender Gasentwicklung am Ende der Reaktion entfernt wird, unbedingt den Schlauch aus der pneumatischen Wanne nehmen! Sonst fließt Wasser durch bei der Abkühlung entstehenden Unterdruck in den noch heißen Kolben und kann für unangenehme Überraschungen sorgen. Beim Auseinandernehmen des dann abgekühlten Kolbens kann noch Wasserstoff entweichen.
Entsorgung:
Der hier entstandene harmlose Abfall mit der geringen Menge Magnesium/-oxid/-chlorid kann am einfachsten in den Abfluss wegespült werden oder in den Hausmüll, nachdem das Magnesium vollständig (!) abreagiert ist.
Erklärung:
Magnesium und Wasser reagieren zu Magnesiumoxid und Wasserstoff:
Mg + H2O ---> MgO + H2
Der Wasserstoff im Reagenzglas verbrennt zu Wasser, das sich an den kälteren Stellen des Reagenzglases niederschlägt:
2 H2 + O2 ---> 2 H2O
Als "brennbare Luft" war das Gas bereits im 16. Jahrhundert durch die Reaktion von Säuren mit Metallen bekannt Erstmals rein dargestellt wurde Wasserstoff vom englischen Chemiker und Physiker Henry Cavendish im Jahre 1766, als er mit Metallen (Eisen, Zink und Zinn) und Säuren experimentierte. Cavendish interpretierte das gewonnene Gas, inflammable air, als die Darstellung des reinen Phlogistons. Er untersuchte das Gas eingehend und veröffentlichte seine Erkenntnisse darüber noch im selben Jahr. 1781 entdeckte und erkannte Cavendish erst, dass Wasserstoff (mit Sauerstoff) zu Wasser verbrennt, dass also Wasser kein Element ist.

Apparatur nach Cavendish
Eine genauere Analyse geschah durch Antoine Laurent de Lavoisier, der dem Wasserstoff auch seinen Namen gab. Der französische Chemiker entdeckte das Gas im Jahr 1787 unabhängig von Cavendish, als er in einem Experiment zeigen wollte, dass bei chemischen Reaktionen keine Masse verloren geht oder erzeugt wird. Er leitete Wasserdampf in einer abgeschlossenen Apparatur über glühende Eisenspäne und ließ ihn an anderer Stelle kondensieren. Dabei stellte er fest, dass die Masse des kondensierten Wassers etwas geringer war als die der ursprünglichen Menge. Dafür entstand ein Gas, dessen Masse zusammen mit dem Gewichtszuwachs des oxidierten Eisens genau der "verlorengegangenen" Wassermenge entsprach. Sein eigentliches Experiment war also erfolgreich.

Versuchsaufbau von Lavoisier
Lavoisier untersuchte das entstandene Gas weiter und führte die heute als Knallgasprobe bekannte Untersuchung durch, wobei das Gas verbrannte. Er nannte es daher zunächst "inflammable air"="brennbare Luft". Als er in weiteren Experimenten zeigte, dass sich aus dem Gas umgekehrt auch Wasser erzeugen lässt, taufte er es hydrogène (griechisch: hydro = Wasser; genes = erzeugend). Das Wort bedeutet demnach: "Wasserbildner"“. Die deutsche Bezeichnung lässt auf die gleiche Begriffsherkunft schließen.
Sein Symbol H stammt aus dem Lateinischen Hydrogenium "Wassererzeuger"; von altgriechisch hydor "Wasser" und gignomai "werden, entstehen". Wasserstoff ist das leichteste aller chemischen Elemente; deshalb steht es im Periodensystem in der 1. Periode und der 1. Gruppe, nimmt also den ersten Platz ein.
Bilder:

Apparatur heute

Auffangen des Gases in einem Reagenzglas
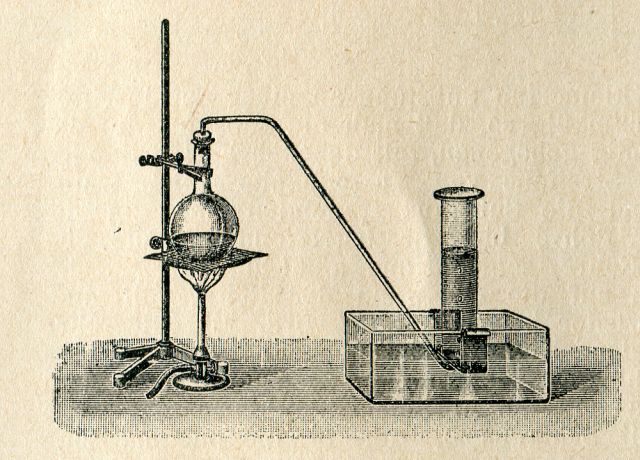
Apparatur anno 1922
Literatur:
"Chemische Schulversuche" zusammengetragen von Prof. Friedr. Brandstätter
Verlag von A. Pichlers Witwe & Sohn Wien 1922
- Kapitel "Wasserstoff" Seite 10 Versuch 4 "Aus Wasser mittels Magnesium" -
Otto Krätz "7000 Jahre Chemie"
Nikol Verlagsgesellschaft mbH & Co. KG Hamburg 1999 ISBN 3-933203-20-1
WIKIPEDIA
