Im folgenden Experiment wird Sauerstoff nach einer wenig bekannten Methode aus Chlorkalk dargestellt. Chlorkalk ist eine Mischung aus Calciumhypochlorit, Calciumchlorid und Calciumhydroxid mit der formalen Summenformel: 3 CaCl(ClO)*Ca(OH)2 *5 H2O, wobei der reaktive Partner das CaCl(ClO) ist.
Geräte:
Weithals-Erlenmeyerkolben 300 ml, Gummistopfen mit Gasableitungrohr und Schlauch, Stativ mit entsprechendem Material, Dreifuß mit Keramik-Drahtnetz, Kartuschen- oder Bunsenbrenner, pneumatische Wanne, Probiergläser / kleinere Standzylinder zum Auffangen des Gases, Waage, Messzylinder, Spatel / Löffel
Chemikalien:
Chlorkalk



Cobalt(II)-nitrat
Sauerstoff
Hinweis: Chlorkalk gast aus und bildet nach einiger Zeit merkliche Mengen an Chlor, daher sollte in einem belüfteten Zimmer oder unter einem Abzug gearbeitet werden. Sauerstoff wirkt oxidierend. Chlorkalk-Aufschlämmungen neigen beim Erwärmen/Erhitzen zum starken Schäumen. Deswegen bitte die Dimensionen des Erlenmeyerkolbens und folgend genannte Mengen zum Ansatz einhalten! Man sollte den Erlenmeyerkolben während des Erwärmens mit der dann schwarzen Aufschlämmung/Schaum unbedingt im Auge behalten.
Durchführung:
In den Erlenmeyerkolben werden 20 g Chlorkalk fein gepulvert vorgelegt und mit 40 ml Wasser durch Schütteln/Schwenken gut aufgeschlämmt. Danach werden 2 Spatelspitzen Cobalt(II)nitrat zugegeben und der Kolben mit vorbereitetem Gummistopfen und Gasableitungsrohr/Schlauch verschlossen. Der Schlauch soll ins Wasser der gefüllten pneumatischen Wanne reichen. Während der Zugabe des Cobaltnitrates und anschließendem leichten Schütteln/Schwenken setzt die Reaktion meistens schon bei Raumtemperatur ein und der Inhalt des Kolbens wird schwarz.
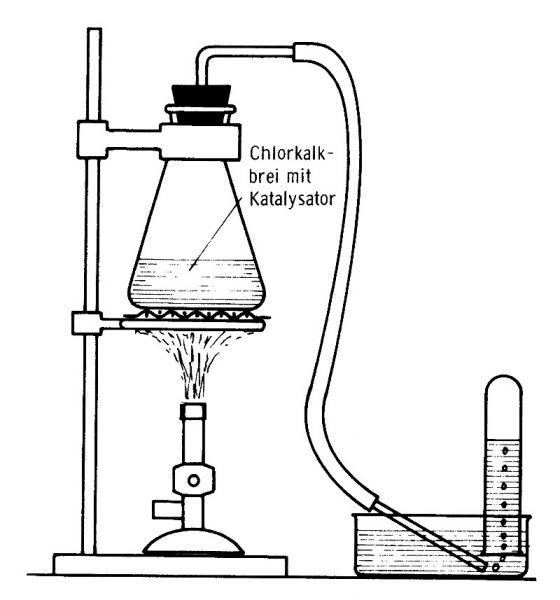
Die Apparatur als Skizze (Zeichnung aus "225 x Chemie – Ein Experimentierbuch“)
Jetzt wird mit kleiner Flamme gelinde erwärmt. Die ersten Anteile sind nur viel Luft (Volumen des Erlenmeyerkolbens) und werden verworfen. Wenn eine gleichmäßige Gasentwicklung einsetzt, wird das Gas in Probiergläsern bzw. Standzylindern pneumatisch aufgefangen.
Bevor der Brenner wegen nachlassender Gasentwicklung am Ende der Reaktion entfernt wird, ist der Schlauch unbedingt aus der pneumatischen Wanne zu entnehmen! Ansonsten fließt Wasser durch den bei der Abkühlung entstehenden Unterdruck in den noch heißen Kolben und kann zu Temperaturspannungen bis hin zum Platzen des Reaktionsgefäßes führen. Alternativ kann auch der Gummistopfen mit dem Gasbleitungsrohr / Schlauch entfernt werden und der Kolben so belüftet und dann der Brenner entfernt werden. Diese zuletzt genannte Vorgehensweise ist vor allem dann empfehlenswert, wenn Schaum in das Gasableitungsrohr und den Schlauch gelangt ist.
Ein glimmender Holzspan, in das Auffanggefäß gehalten, sollte sofort hell aufflammen (Glimmspanprobe).
Erklärung:
Cobalt(II)-salze werden durch Chlorkalklösung zunächst zu schwarzem Cobalt(III)-hydroxid (Co(OH)3) oxidiert, welches für die katalytische Zersetzung des Calciumhypochlorits zu Calciumchlorid und Sauerstoff verantwortlich ist:
2 CaCl(ClO) ---> 2 CaCl2 + O2
Entsorgung:
Die cobalthaltige Aufschlämmung/Lösung wird in einen Sammelbehälter für Schwermetallabfälle gefüllt und der Deckel bis zur vollständigen Zersetzung des Chlorkalks nicht (!) fest verschlossen (kann einige Tage dauern).
Alternative Katalysatoren:
Die Einstufung von Cobaltsalzen als CMR-Stoffe in Kategorie 1 und 2 (T+/ T statt bisher Xn je nach Anion) gemäß Tabelle 3 des Anhangs VI der Verordnung (EG) Nr. 1272/2008 (CLP-Verordnung) sowie der 1. Anpassung der Verordnung (790/2009) läßt die Abgabe an Privatpersonen praktisch nicht mehr zu. Als Alternative schlägt das von mir zitierte Experimentierbuch Kupferoxid vor.
Fotos:

Durch Erwärmen stark aufgeschäumter Chlorkalk-Schlamm mit schwarzem Cobalt(III)-hydroxid.

Man sieht deutlich, wie stark Chlorkalk-Aufschlämmungen zum Schäumen neigen.
Literatur:
"225 x Chemie – Ein Experimentierbuch“ von Kurt Waselowsky
Franckh´sche Verlagshandlung W. Keller & Co. 1982 – ISBN 3 440 05045 9
Seite 34, Versuch 5.4

