Anissäure bzw. p-Methoxybenzoesäure gehört zu den aromatischen Carbonsäuren und kommt natürlich in vielen Pflanzen vor, naheliegenderweise vor allem im Anis. Für dessen charakteristischen Duft ist allerdings nicht die Anissäure, sondern u.a. das trans-Anethol und der Anisaldehyd verantwortlich. Letzterer dient in dieser Synthese als Edukt. Der süßlich-aromatisch nach Waldmeister riechende Aldehyd neigt, ebenso wie Benzaldehyd oder auch Vanillin, zur Oxidation und bildet dabei die entsprechende Carbonsäure. In diesem Versuch wird die Oxidation mit Kaliumpermanganat im Basischen vollzogen. Anissäure kann z.B. weiter zu Estern verarbeitet werden. Die vorliegende Vorschrift soll eine von weiter folgenden sein, die sich mit der Herstellung verschiedener Duftstoffe (vor allem "vanilloider" Duftstoffe) beschäftigen.
Geräte:
250 mL Rundkolben, Rückflusskühler (optional), Magnetheizrührer, Rührfisch, Erlenmeyerkolben und Bechergläser, Petrischale.
Chemikalien:
Anisaldehyd

Kaliumpermanganat



Natriumhydroxid

Schwefelsäure 1M

Natriumsulfit
p-Methoxybenzoesäure

Hinweis: In den genannten Mengen kann die Reaktion ohne Rückflusskühler durchgeführt werden. Bei up-scaling ist allerdings auf bessere Sicherheitsvorkehrungen zu achten, da die Oxidation mit Kaliumpermanganat erfahrungsgemäß auch durchgehen kann.
Durchführung:
In einen 250 mL Rundkolben werden 6,80 g (0,05 mol) Anisaldehyd pipettiert und ein Rührfisch hinzugegeben. Dann wird eine Lösung von 7,9 g (0,05 mol, theoretisch 50% Überschuss) Kaliumpermanganat in 150-200 mL Wasser bereitet. In dieselbe Lösung werden auch 5 g (0,125 mol) Natriumhydroxid gegeben. Die warme, alkalische Permanganatlösung wird unter starkem Rühren zum Aldehyd gegeben. Nach ca. 30 Sekunden beginnt die Mischung grünlich zu werden (Manganat), danach beginnt Braunstein auszufallen. Nachdem eine Stunde gerührt wurde, wird noch einmal genauso lange auf 80-90 °C erhitzt. Danach lässt man abkühlen und gibt der noch immer pinken Suspension solange eine konzentrierte Natriumsulfit-Lösung zu, bis die violette Färbung verschwindet (Pipette!). Schließlich wird vom Braunstein abfiltriert und das klare Filtrat mit ca. 100 mL 1 M Schwefelsäure angesäuert. Sofort nach der Zugabe fällt ein Niederschlag aus. Dieser wird abfiltriert, mit ausgiebig Wasser gewaschen und aus einem Liter dest. Wasser umkristallisiert. Nach der Trocknung ergeben sich Benzoesäure-artige Kristalle.
Ausbeute: 5,44 g (72 % d.Th.) farblose Kristalle. Geruch: Benzoesäure-ähnlich, allerdings eher unaufdringlicher und süsslicher.
Entsorgung:
Alle mangan-haltigen Lösungen kommen in den Schwermetallabfall. Alles andere kann in neutralisierter Form in den Abfluss gegeben werden.
Erklärung:
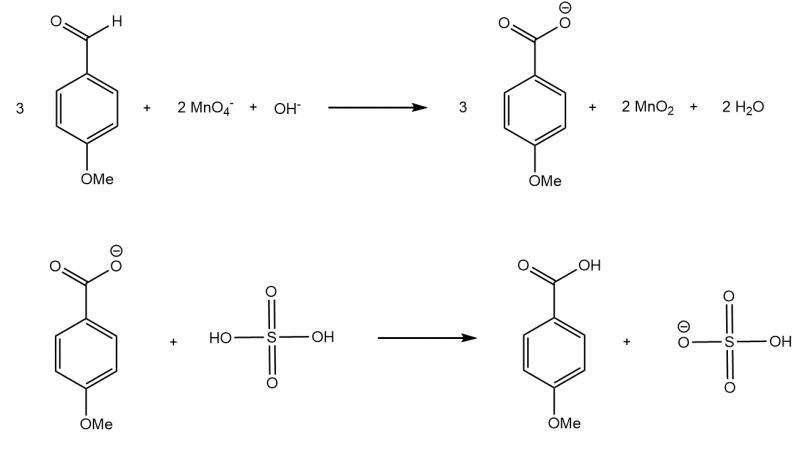
Kaliumpermanganat oxidiert den Aldehyd zur Carbonsäure. Da die Reaktionen im Basischen durchgeführt wird, entsteht als Reaktionsprodukt Braunstein. Nach Ansäuern fällt die freie Carbonsäure aus, die in kaltem Wasser quasi nicht löslich ist. Die verwendete Menge Schwefelsäure fiel deutlich höher aus, als eigentlich nötig wäre. Jedoch ist diese günstig und ein saures Medium für das Ausfallen des Produkts zu bevorzugen.
Bilder:

Reaktionsmischung nach den ersten Minuten

Mit Sulfit versetzte Mischung

Ausfallendes Produkt

Umkristallisieren

Trockenes Produkt