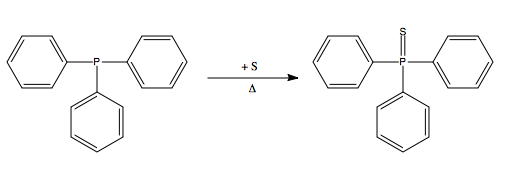
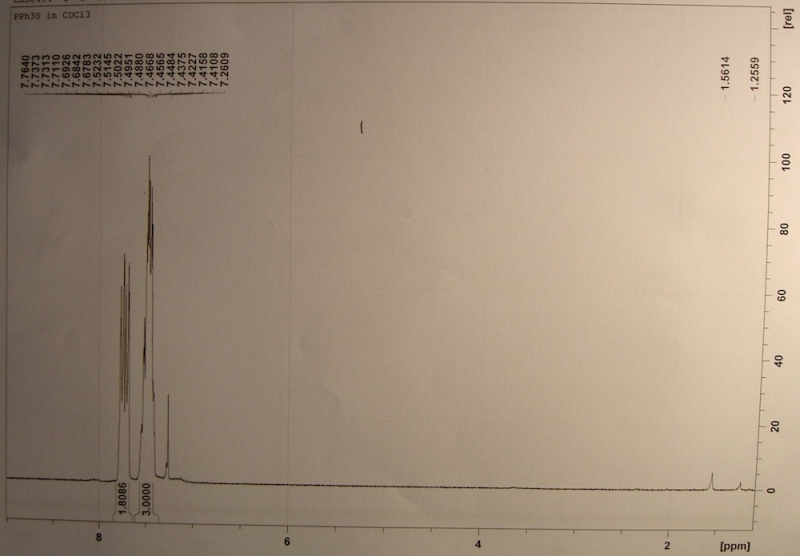
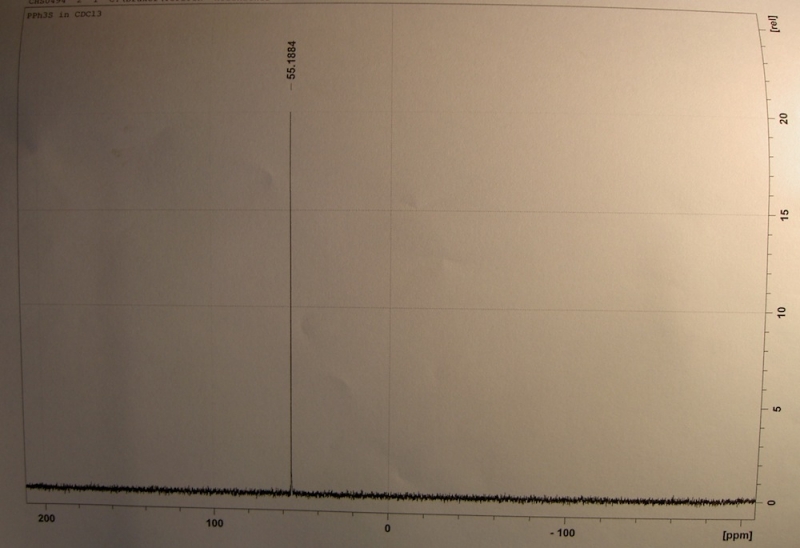
Triphenylphosphin
(Triphenylphosphan, TPP). (H5C6)3P, C18H15P, MG. 262,28. Farblose, monokline, tribolumineszierende Prismen, D. 1,075 (80°), Schmp. 80°, Sdp. >360°, 188° (1,3 hPa), unlösl. in Wasser, lösl. in Alkohol, leicht lösl. in den meisten org. Lösungsmitteln. T. ist das bekannteste der org. Phosphine; nach der IUPAC-Regel R-2.0 (von 1989) wird die Verb. Triphenylphosphan genannt. Man kann sie als eine Art Propeller-Molekül auffassen.
Herst.: Durch Einwirkung von Phenylmagnesiumbromid auf Phosphortrichlorid.
Verw.: In der org. präparativen Chemie zus. mit Tetrachlormethan zur Chlorierung, Dehydratisierung, P–N-Verknüpfung, Peptid-Synth. etc., als Polymerisations-Initiator für Olefine, Aldehyde u. aktivierte Vinyl-Verbindungen. Bei Kondensationsreaktionen, z.B. bei der Synth. von Peptiden, Nucleotiden u. Makroliden, kann es als Sauerstoff-Akzeptor zus. mit dem Wasserstoff aufnehmenden Di-(2-pyridyl)-disulfan eingesetzt werden. In der Technik wie auch im Labor ist T. Ausgangsstoff für die Herst. der Ylide (Wittig-Reaktion), ferner dient es als Stabilisator u. Inhibitor sowie zur Desoxygenierung von Peroxiden u.a. Oxiden, wobei T. selbst in Triphenylphosphinoxid (C18H15OP, MG. 278,29, D. 1,2124, Schmp. 157°, Sdp. >360°, in siedendem Wasser etwas lösl.) übergeht; diese Reaktion nutzt man im Laboratorium zur Red. evtl. explosibler Peroxide von zu destillierenden Lösungsmitteln. Tris(triphenylphosphin)-Cobaltdihydrid war der erste zur Stickstoff-Fixierung befähigte Metallkomplex.
Lit.: Angew. Chem. 87, 863–874 (1975); 88, 111–120 (1976) ï Beilstein EIV 16, 951, 1011 ï Chem. Ber. 108, 2680–2692 (1975) ï J. Am. Chem. Soc. 106, 3682 (1984); 107, 5812 (1985) ï J. Org. Chem. 42, 2190 (1977) ï Merck-Index (11.), Nr. 9657 ï Synthesis 1981, 1–28 ï Synthetica 1, 510–517 ï Ullmann (4.) 18, 379, 394; 20, 142 ï s.a. Phosphine.
E triphenylphosphine
F triphénylphosphine
I = S trifenilfosfina
Z 2931.00
CAS 603-35-0
Quelle: CD Römpp Chemie Lexikon – Version 1.0, Stuttgart/New York: Georg Thieme Verlag 1995
Wäre also eigentlich recht einfach zu bewerkstelligen

"...wie ein Sprecher betont,hat für die Bevölkerung zu keinem Zeitpunkt Gefahr bestanden."
"...mittlerweile rostet das Miststück..." E.v. Däniken