Fullerene zeigen eine reichhaltige Chemie, wobei sie teils wie Aromaten (Birch-Reduktion), teils wie Alkene (Additionen) reagieren. Hier wird die Addition von Brom an [60]Fulleren beschrieben. Das Produkt weist hohe Symmetrie auf (Punktgruppe Th), was die Nomenklatur der Verbindung sehr vereinfacht, da hier statt der Angabe der Position aller 24 Substituenten die Angabe der Punktgruppe zur eindeutigen Benennung ausreicht.1 Bemerkenswert ist auch die durch die Addition eintretende Farbänderung: Durch Zerstörung des konjugierten π-Elektronensystems ändert sich die Farbe von tiefviolett zu hellgelb.
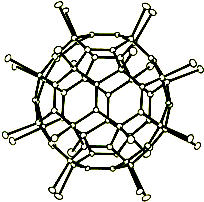
Strukturformel von Th-C60Br24 (1)
Geräte:
Becherglas 50 mL, Magnetrührer
Chemikalien:
(60)Fulleren
Brom
Diethylether
Tetraeicosabrom-(60)fulleran
Durchführung:
Abzug!
[60]Fulleren (10,0 mg, 13,9 µmol) wird mit Brom (5 mL, 100 mmol) bei 30°C eine Stunde gerührt. Dann wird bei 40°C so lange weitergerührt, bis das Brom vollständig verdampft ist. Der orangegelbe Rückstand wird mit Diethylether (5 mL) nachgewaschen und getrocknet. Ausbeute annähernd quantitativ. Hellgelbes Pulver.
Entsorgung:
Brom wird mit Natriumthiosulfatlösung unschädlich gemacht. [60]Fulleren und das Produkt sollten aufgearbeitet werden oder werden den organischen Abfällen zugeführt. Diethylether wird zu den halogenfreien organischen Lösemittelabfällen gegeben.
Erklärung:
Das Brom addiert an das [60]Fulleren:
C60 + (12+n) Br2 ---> Th-C60Br24 * n Br2
Literatur:
(1) Tebbe, F., et al., Synthesis and Single-Crystal X-ray Structure of a Highly Symmetrical C60 Derivative, C60Br24, Science 256 (5058), 1992, 825.
Bilder:

10,0 mg [60]Fulleren

Bromierung

Rohprodukt

Probe des reinen Th-C60Br24