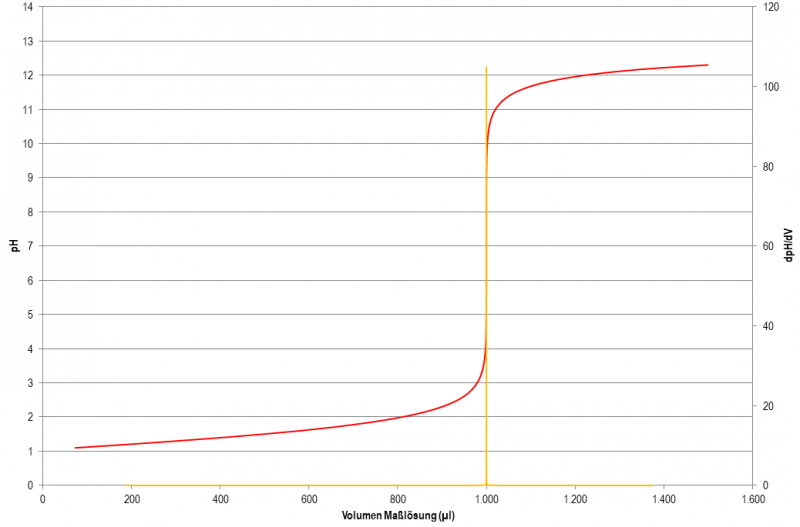
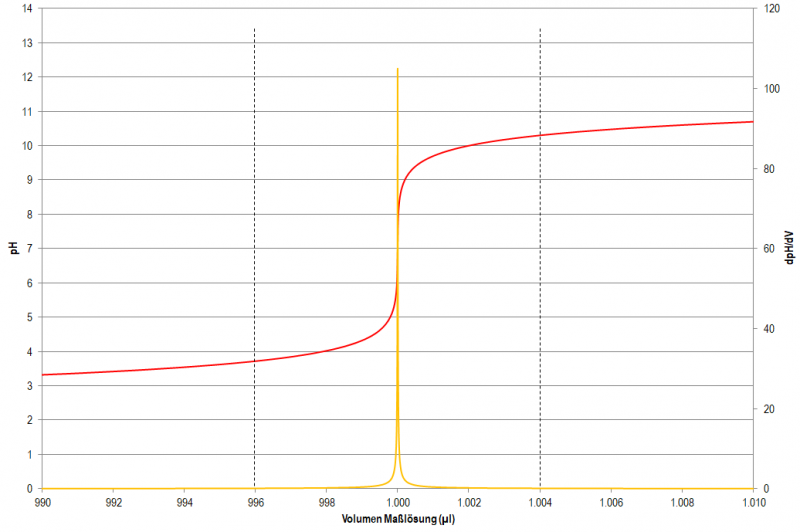
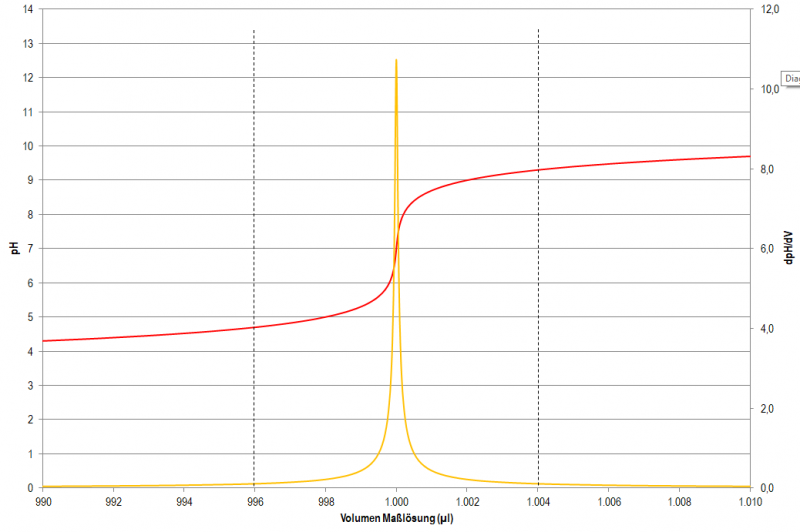
Wenn für Titrationen nur eine kleine Probenmenge zur Verfügung steht oder aufgrund niedriger Konzentrationen der Verbrauch einer nur geringen Menge an Maßlösung zu erwarten ist, dann bietet sich eine Mikro-Titration an. Mit einer 25 ml Standard-Bürette Klasse AS ist eine Genauigkeit von 0,025 ml möglich, die Limitationen liegen hier sowohl in der Ablesbarkeit des Verbrauchs als auch in der aus dem Hahn dosierbaren Tropfengröße. bei Verbrauch von nur 1 ml Maßlösung sind das bereits 2,5% relativer Fehler. Und natürlich gibt es bei der Bürette noch eine Menge weiterer ungünstiger Einflussfaktoren - Temperaturfehler (im Bereich 15 - 25°C ca. 0,1% Ausdehnung von Wasser auf 5°C) und vor allem Nachlauffehler des Flüssigkeitsfilms in der Bürette der immer größer wird je kleiner der Durchmesser - wann ist der richtige Zeitpunkt zum Ablesen?
Wenn es um kleine Flüssigkeitsvolumina geht, dann kann man Mikrobüretten (z.B. nach Bang) benutzen - bei der kleinsten handelsüblichen Ausführung hat man dann eine Teilung von 0,01 ml - somit ist wieder etwa 1% Genauigkeit möglich. Solche Geräte kosten um die 100 EUR und das Handhaben der Flüssigkeit ist wegen der Kapillarkräfte teils etwas schwierig. Rehberg[1] hat 1925 einen Apparat vorgeschlagen bei dem man mittels einer Stellschraube und einer Hg-Säule von unten die Maßlösung dosieren kann, damit konnte er durch eine Kapillarspitze die direkt in die zu analysierende Flüssigkeit taucht die Maßlösung auf 1 µl genau dosieren, die Ablesung erfolgte nach wie vor an einer Kapillare mit Markierungen für die Volumeinheiten.
Ein entscheidender Faktor für die praktisch erzielbare Genauigkeit ist die Tropfengröße die man dosieren kann. Diese ist vor allem abhängig von der Oberflächenspannung und dem Durchmesser der Öffnung:
mgf = dπγ
Mit: m = Masse des abreißenden Tropfens; g = Gravitationskonstante; f = experimenteller Korrekturfaktor; d = Durchmesser der Öffnung; γ = Oberflächenspannung. Nach diesem Zusammenhang können z.B durch Auswiegen einer bestimmten Anzahl Tropfen und Vergleich mit einer bekannten Substanz auch auf einfache Weise Oberflächenspannungen gemessen werden.
Je kleiner die Öffnung, desto kleiner auch der Tropfen. Relativ große Glashähne mit ihren dicken Spitzen aus denen Flüssigkeit nur unter ihrem eigenen Gewichtsdruck heraustropft sind daher prinzipiell bald an ihrer Grenze. Eine einfache Möglichkeit bieten hier Einweg-Spritzen zur subkutanen Injektion von Insulin für Diabetes-Patienten. Für eine möglichst komfortable und schmerzfreie Injektion werden dabei Nadeln mit einem Durchmesser von typisch 0,33 mm eingesetzt (bei entsprechend geringerem Innendurchmesser). Deren aufgedruckte Skala ist natürlich für analytisch präzises Arbeiten ungeeignet, aber durch Auswiegen des Verbrauchs kann dieses kleine Manko sehr gut ausgeglichen werden - mit einer Analysenwaage sind so nochmal deutlich bessere Genauigkeiten möglich als mit jedem volumetrischen Gerät! Der Edelstahl aus dem die Nadeln bestehen sollte auch ausreichend inert sein gegen die üblichen Maßlösungen.
Einen ähnlich gelagerten Vorschlag zur Verwendung medizinischer Spritzen haben bereits 1936 Szebellédy & Clauder gemacht[2], warum diese Methodik heute nicht gängiger ist, ist nicht verständlich.
Geräte:
U 100 Insulinspritze (1 ml), Reagenzglas, Analysenwaage
Optional: Pyknometer, Magnetrührer
Chemikalien:
Natronlauge 0,1 mol/l

Salzsäure 0,1 mol/l

Indikator (hier z.B: Mischindikator nach Mortimer; Bromkresolblau - Methylrot 3:1 in EtOH)
Durchführung:
1. Ermittlung der durchschnittlichen Tropfengröße:
Die Spritze wurde mit dest. Wasser gefüllt, gewogen und es wurden mehrfach Portionen von 20 Tröpfchen abgegeben und die Gewichtsabnahme ermittelt. Je nachdem wie man die Spritze dabei genau hält und wie rasch man drückt wurden dabei Tropfengrößen von 3,9 - 5,6 µl ermittelt, typisch sollten etwa 4 µl sein. Somit ist bei einem Verbrauch von 1 ml Maßlösung eine Genauigkeit von besser als 0,5% möglich, durch Abstreifen an der Glaswand wären auch kleinere Teile dosierbar. Die Wägegenauigkeit der Analysenwaage von 0,1 mg ist dabei jedenfalls sicher nicht der limitierende Faktor.
2. Titration von HCl mit NaOH:
In einem kleinen, tarierten 11 mm Reagenzglas wurde ca. 1 ml der 0,1 molaren HCl (Faktor wurde früher schon mal zu 1,038 bestimmt) vorgelegt und genau eingewogen, dann ebenfalls aus einer Spritze ein kleines Tröpfchen Indikatorlösung zugesetzt und schließlich mit der 0,1 molaren NaOH (Faktor 0,998) aus der Spritze bis zum Umschlag nach blau titriert. Die Spritze wurde dazu beliebig vollgesogen, genau gewogen und aus der Gewichtsdifferenz der Verbrauch ermittelt. Aus Gründen des Komforts wurde dabei ein kleines Magnetrührstäbchen benutzt, das ist aber optional. Es empfiehlt sich auf jeden Fall, dazwischen mehrfach umzuschwenken um sicherzustellen dass Tröpfchen, die an der Reagenzglaswand haften auch sicher mit erfasst werden. Ebenfalls wichtig ist, die Spritze nach dem Befüllen und vor dem Wiegen außen gut abzutrocknen falls noch Tröpfchen anhaften - diese könnten sonst verdunsten oder abgeschmiert werden und so einen Verbrauch vortäuschen. Ebenfalls sollte ein Tröpfchen das nach Ende der Titration noch an der Spitze haftet wieder eingesogen werden.
Die drei Bestimmungen ergaben für die HCl folgende Werte (mol/l):
0,1036 - 0,1035 - 0,1036 / Mittelwert: 0,1036
Die Abweichungen der einzelnen Messwerte vom Mittelwert betragen weniger als 0,1%, das ist eine hervorragende Wiederholgenauigkeit, ähnlich wie Szebellédy & Clauder sie gefunden haben! Auch der Absolutwert ist in sehr guter Übereinstimmung mit dem früher bestimmten Faktor der Maßlösung.
Erklärungen:
NaOH + HCl ---> NaCl + H2O
Die Dichte von so verdünnten Lösungen kann in guter Näherung mit 1 angenommen werden und mol/l und mol/kg gleichgesetzt werden. Eine Messung im Pyknometer ergab Werte von 0,9998 für die HCl und 1,0024 für die NaOH. Damit lassen sich die erhaltenen Gewichtswerte für höchste Genauigkeit auch in Volumskonzentrationen umrechnen. Idealerweise geht man bei solchen Titrationen aber schon von einer Maßlösung aus bei der ein Urtiter eingewogen und auf Gewicht statt Volumen aufgefüllt wurde (Einheiten generell in mol/kg statt mol/l).
In Summe ergibt sich somit eine sehr einfache Möglichkeit mit einfachen Geräten eine Titration im Maßstab 0,2 - 1 ml mit hoher Genauigkeit durchzuführen.
Entsorgung:
Die Lösungen können direkt zum Abwasser gegeben werden.
Bilder:

Einwiegen der HCl

Dosierung von Indikator

Vorlage im Reagenzglas

Insulinspritze mit NaOH

Einwiegen der Spritze
Video: der Letzte Tropfen zum Umschlag
Literatur:
[1] A Method of Microtitration; P. B. Rehberg, Biochemical Journal (1925), 19(2), 270-277
[2] Mikro-Maßanalyse mittels Gewichtsbürette; Szebellédy, L. & Clauder, O. Fresenius, Zeitschrift f. anal. Chemie (1936), 105, 26